题目内容
下列叙述正确的是
- A.CO的摩尔质量为44 g?mol-1
- B.某物质的摩尔质量在数值上等于该物质的相对分子质量或相对原子质量
- C.3.01×1023个N2分子的质量为14g
- D.标准状况下,1 mol任何物质的体积均为22.4L
C
分析:A、依据原子摩尔质量计算分子摩尔质量;
B、微粒摩尔质量是以g/mol为单位,数值上近似等于微粒相对质量的数值;
C、依据n= ,m=nM计算分子的质量;
,m=nM计算分子的质量;
D、依据气体摩尔体积的应用条件是标准状况下的气体计算分析.
解答:A、CO的摩尔质量为28 g?mol-1,故A错误;
B、摩尔质量表述为:以g/mol为单位,在数值上等于该微粒的相对原子质量或相对分子质量,故B错误;
C、3.01×1023个N2分子物质的量=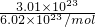 =0.5mol,分子的质量=0.5mol×28g/mol=14g,故C正确;
=0.5mol,分子的质量=0.5mol×28g/mol=14g,故C正确;
D、标准状况下,1 mol任何气体的体积约为22.4L,故D错误;
故选C.
点评:本题考查了摩尔质量、微粒物质的量、气体摩尔体积的条件应用,理解概念是解题关键,题目较简单.
分析:A、依据原子摩尔质量计算分子摩尔质量;
B、微粒摩尔质量是以g/mol为单位,数值上近似等于微粒相对质量的数值;
C、依据n=
 ,m=nM计算分子的质量;
,m=nM计算分子的质量;D、依据气体摩尔体积的应用条件是标准状况下的气体计算分析.
解答:A、CO的摩尔质量为28 g?mol-1,故A错误;
B、摩尔质量表述为:以g/mol为单位,在数值上等于该微粒的相对原子质量或相对分子质量,故B错误;
C、3.01×1023个N2分子物质的量=
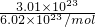 =0.5mol,分子的质量=0.5mol×28g/mol=14g,故C正确;
=0.5mol,分子的质量=0.5mol×28g/mol=14g,故C正确;D、标准状况下,1 mol任何气体的体积约为22.4L,故D错误;
故选C.
点评:本题考查了摩尔质量、微粒物质的量、气体摩尔体积的条件应用,理解概念是解题关键,题目较简单.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
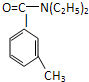 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH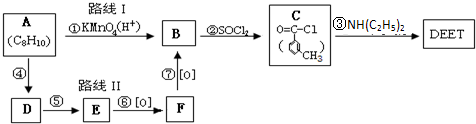


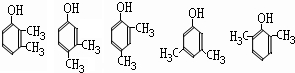 (任写2种)
(任写2种)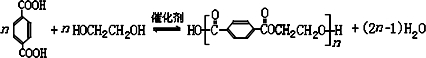

 NH3?H2O+H+
NH3?H2O+H+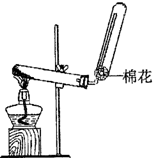 (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.