题目内容
【题目】用下图装置加以必要的导线连接后达到粗铜精炼的目的。

⑴A烧杯是________________(填〝电解池〞或〝原电池〞),
B烧杯是________________(填〝电解池〞或〝原电池〞)。
⑵其中Zn接B烧杯中的___________,(填“粗铜”或“纯铜”),B烧杯中应该盛____________溶液。
⑶分别写出石墨棒和纯铜棒的电极反应式
石墨棒:____________________________________,
纯铜棒:____________________________________。
⑷若锌减少了0.65 g,则纯Cu的质量增加了________g。
【答案】原电池 原解池 纯铜 CuSO4或其它易溶性的铜盐 2H++2e-=H2↑ Cu2++2e-=Cu 0.64
【解析】
(1)根据原电池和电解池的构成条件来分析;
(2)电解精炼铜时,电解质溶液是含有铜离子的盐;
(3)根据电解池和原电池的工作原理来书写电极反应;
(4)根据电极反应和电子守恒来计算。
(1)A烧杯含有两个活泼性不同的电极,有自发的氧化还原反应,形成了闭合回路,存在电解质溶液,属于原电池装置,B烧杯就存在了外加电源,属于电解装置;
因此,本题正确答案是:原电池;电解池;
(2)电解精炼铜时,粗铜做阳极,与电源的正极相连,纯铜做阴极,与电源的负极相连;电解质溶液必须是含有铜离子的可溶性的盐,如硫酸铜溶液或其它易溶性的铜盐等;
因此,本题正确答案是: 纯铜;CuSO4或其它易溶性的铜盐;
(3)石墨棒是原电池的正极,发生电极反应为: 2H++2e-=H2↑;纯铜棒是电解池的阴极,
电极反应为: Cu2++2e-=Cu;
因此,本题正确答案是: 2H++2e-=H2↑;Cu2++2e-=Cu;
(4)在A烧杯中,金属锌电极发生的电极反应为:Zn-2e-=Zn,若锌减少了0.65 g即0.01mol时,转移电子为0.02mol,在B烧杯中,纯铜电极发生的反应为: Cu2++2e-=Cu,当转移0.02mol电子时,则析出金属Cu的物质的量为0.01mol,质量为0.64g;
因此,本题正确答案是:0.64。

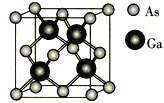
【题目】GaN是制造5G芯片的材料,氮化镓铝和氮化铝LED可发出紫外光。回答下列问题:
(1)基态As原子核外电子排布式为[Ar]________,下列状态的铝中,电离最外层的一个电子所需能量最小的是_____________(填标号)。
A. ![]() B.
B. ![]() C.[Ne] D.
C.[Ne] D. ![]()
(2)8—羟基喹啉铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与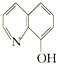 (8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为_______;
(8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为_______; 所含元素中电负性最大的是___(填元素符号),C、N、O的杂化方式依次为 _____、_________和____________。
所含元素中电负性最大的是___(填元素符号),C、N、O的杂化方式依次为 _____、_________和____________。
(3)已知下列化合物的熔点:
化合物 | AlF3 | GaF3 | AlCl3 |
熔点/℃ | 1040 | 1000 | 194 |
①表中卤化物的熔点产生差异的原因是____________。
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6,二聚体Al2Cl6的结构式为_______;其中Al的配位数为_________。
(4)GaAs的晶胞结构如图所示,紧邻的As原子之间的距离为x,紧邻的As、Ga原子之间的距离为y,则![]() =________。
=________。