题目内容
【题目】(1)在臭氧发生器中装入100mLO2,经反应3O2=2 O3,最后气体体积变为95mL(体积均为标准状况下测定),则反应后混合气体的密度为____________。
(2)将溶质质量分数为a%NaOH溶液蒸发掉m g水后,变成VmL 2a%的NaOH不饱和溶液,则蒸发后的溶液的物质的量浓度是__________。
(3)amolH2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为_______。
(4)现有CO、CO2、O3(臭氧)三种气体,它们分别都含有1mol氧原子,则三种气体的质量之比为________(最简整数比)。
(5)标准状况下,密度为0.75g/L 的NH3与CH4组成的混合气体中,NH3的体积分数为__________,该混合气体对氢气的相对密度为_____________。
【答案】1.5 g·L1 ![]() mol/L b/4a 14:11:8 80% 8.4
mol/L b/4a 14:11:8 80% 8.4
【解析】
(1)反应前氧气的物质的量=![]() =
=![]() mol,故反应前氧气的质量
mol,故反应前氧气的质量![]() mol×32g/mol=
mol×32g/mol=![]() g,根据质量守恒定律可知,反应后混合气体的质量等于反应前氧气的质量,故反应后混合气体的密度=
g,根据质量守恒定律可知,反应后混合气体的质量等于反应前氧气的质量,故反应后混合气体的密度=![]() =1.5g/L;
=1.5g/L;
(2)令蒸发后溶液的质量为xg,浓缩蒸发前后溶质的质量不变,则:(x+m)g×a%=x×2a%,解得x=m,NaOH的质量为mg×2a%=2am% g,所以NaOH的物质的量为![]() =
=![]() mol,蒸发后所得溶液体积为VL,所以蒸发后溶液的物质的量浓度为
mol,蒸发后所得溶液体积为VL,所以蒸发后溶液的物质的量浓度为![]() =
=![]() mol/L;
mol/L;
(3)一个硫酸分子中含有四个氧原子,所以含有b个氧原子的硫酸的分子数是![]() ,NA=
,NA=![]() =
=![]() =
=![]() ;
;
(4)CO、CO2、O3三种气体,它们含有的氧原子个数之比为1:2:3,则氧原子的物质的量相同,设都为1mol,则n(CO)=1mol,n(CO2)=![]() mol,n(O3)=
mol,n(O3)=![]() mol,则这三种气体的质量之比为1mol
mol,则这三种气体的质量之比为1mol![]() 28g/mol:
28g/mol:![]() mol
mol![]() 44g/mol:
44g/mol:![]() mol
mol![]() 48g/mol =14:11:8;
48g/mol =14:11:8;
(5)标准状况下,密度为0.75gL-1的NH3与CH4组成的混合气体的平均摩尔质量为:M=0.75gL-1×22.4L/mol=16.8g/mol,设混合气体中NH3、CH4的物质的量分别为x、y,则:![]() =16.8,整理可得:x:y=4:1,相同条件下气体体积之比等于物质的量之比,则混合气体中NH3的体积分数为:
=16.8,整理可得:x:y=4:1,相同条件下气体体积之比等于物质的量之比,则混合气体中NH3的体积分数为:![]() ×100%=80%;混合气体的平均摩尔质量为16.8,该混合气体对氢气的相对密度为
×100%=80%;混合气体的平均摩尔质量为16.8,该混合气体对氢气的相对密度为![]() =8.4。
=8.4。

 黎明文化寒假作业系列答案
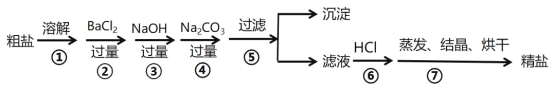
黎明文化寒假作业系列答案【题目】某地湖盐中含有Ca2+、Mg2+、Fe3+、SO42-等杂质离子,氨碱厂用该地湖盐制取烧碱。其中制得精制食盐水的过程如下:

(1)过程Ⅰ中将粗盐加水溶解需要适当加热,其目的是____________________________。
(2)过程Ⅱ的目的是除去SO42-,加入的X溶液是________________________。
(3)下表是过程Ⅱ、Ⅲ中生成的部分沉淀及其在20℃时的溶解度[g/(100gH2O):
CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 | Fe(OH)3 |
2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 | 4.8×10-9 |
①过程Ⅲ中生成的主要沉淀除CaCO3和Fe(OH)3外还有_______________________。
②过程Ⅳ中调节pH时发生的主要反应的离子方程式为_________________________________。
(4)上述精制食盐水中还含有微量的I-、IO3-、NH4+、Ca2+、Mg2+,除去这些离子及进行电解的流程如下:
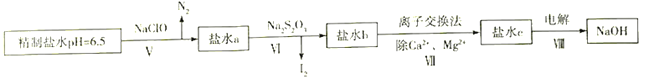
①过程Ⅴ生成N2的离子方程式为__________________________________。
②过程Ⅵ可以通过控制Na2S2O3的量,将IO3-还原为I2,且盐水b中含有SO42-,该过程中发生氧化还原反应,其中氧化剂和还原剂的物质的量之比为________________________________。
③在过程Ⅳ中所用的Na2S2O3俗称海波,是一种重要的化工原料。商品海波主要成分是Na2S2O3·5H2O。为了测定其含Na2S2O3·5H2O的纯度,称取8.00 g样品,配成250 mL溶液,取25.00 mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.050 0 mol·L-1的碘水滴定(发生反应2S2O32-+I2==S4O62-+2I-),下表记录滴定结果:
滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
第一次 | 0.30 | 29.12 |
第二次 | 0.36 | 30.56 |
第三次 | 1.10 | 29.88 |
计算样品的纯度为________________________________。