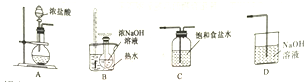
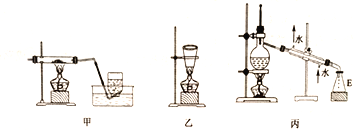
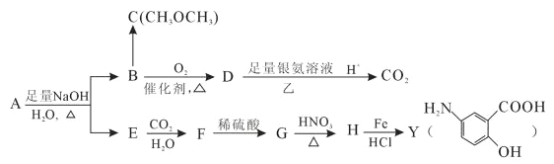
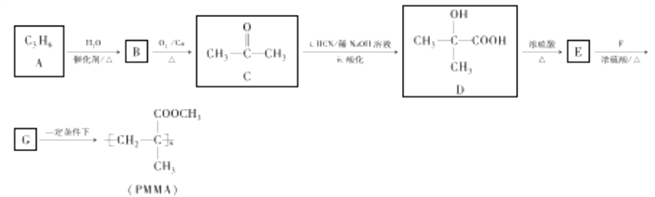
��Ŀ����
����Ŀ��������ij�л���ϳɷ�Ӧ������ͼ�� 
��֪����Һ��ʯ����Һ��죮��ش��������⣺
��1���л�����й����ŵ�����Ϊ ��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ����Ӧ����
��Ӧ�� �� ��
��Ӧ�� �� ��
��3��![]() ����ʵ����Ҫ����������ɣ�д����һ����Ӧ�Ļ�ѧ����ʽ �� �ڶ��������Լ���Ŀ���� ��
����ʵ����Ҫ����������ɣ�д����һ����Ӧ�Ļ�ѧ����ʽ �� �ڶ��������Լ���Ŀ���� ��
��4�����ж���ͬ���칹�壬���з�������������ͬ���칹�干���֣�д�����б�����һ�ȴ��������ֵ��л���Ľṹ��ʽ ��
a����FeCl3��Һ��ɫb���ܷ���������Ӧ��ˮ�ⷴӦc��������ֻ��2��ȡ������
���𰸡�
��1���ǻ����Ȼ�
��2��2  +O2
+O2 ![]() 2
2  ��������Ӧ��
��������Ӧ�� +NaOH
+NaOH ![]()
 +NaCl+H2O����ȥ��Ӧ
+NaCl+H2O����ȥ��Ӧ
��3�� +2NaOH
+2NaOH ![]()
 +NaBr+H2O���Լ������ᣬĿ���ǽ������ữ���ɶ�Ӧ����
+NaBr+H2O���Լ������ᣬĿ���ǽ������ữ���ɶ�Ӧ����
��4��6�� ��
�� 
���������⣺��1���������Ϸ�������Ϊ  ������й����ŵ�����Ϊ�ǻ����Ȼ������Դ��ǣ��ǻ����Ȼ�����2����Ӧ��
������й����ŵ�����Ϊ�ǻ����Ȼ������Դ��ǣ��ǻ����Ȼ�����2����Ӧ�� 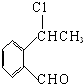 ����������Ӧ���ɼ�Ϊ
����������Ӧ���ɼ�Ϊ  ������ʽΪ��2
������ʽΪ��2  +O2
+O2 ![]() 2
2  ����Ӧ����Ϊ������Ӧ����Ӧ����
����Ӧ����Ϊ������Ӧ����Ӧ����  ������ȥ��Ӧ����
������ȥ��Ӧ����  ������ʽΪ��
������ʽΪ��  +NaOH
+NaOH ![]()
 +NaCl+H2O����Ӧ����Ϊ��ȥ��Ӧ��
+NaCl+H2O����Ӧ����Ϊ��ȥ��Ӧ��
���Դ��ǣ�2  +O2
+O2 ![]() 2
2  ��������Ӧ��
��������Ӧ�� +NaOH
+NaOH ![]()
 +NaCl+H2O����ȥ��Ӧ����3���������Ϸ�����֪��
+NaCl+H2O����ȥ��Ӧ����3���������Ϸ�����֪��  ��������ˮ�⡢���ữ���ɱ�����һ����Ӧ�Ļ�ѧ����ʽΪ��
��������ˮ�⡢���ữ���ɱ�����һ����Ӧ�Ļ�ѧ����ʽΪ��  +2NaOH
+2NaOH ![]()
 +NaBr+H2O���ڶ��������Լ������ᣬĿ���ǽ������ữ���ɶ�Ӧ���ᣬ
+NaBr+H2O���ڶ��������Լ������ᣬĿ���ǽ������ữ���ɶ�Ӧ���ᣬ
���Դ��ǣ�  +2NaOH
+2NaOH ![]()
 +NaBr+H2O���Լ������ᣬĿ���ǽ������ữ���ɶ�Ӧ�����4���������Ϸ�������Ϊ
+NaBr+H2O���Լ������ᣬĿ���ǽ������ữ���ɶ�Ӧ�����4���������Ϸ�������Ϊ  ��a����FeCl3��Һ��ɫ��˵�����з��ǻ���b���ܷ���������Ӧ��ˮ�ⷴӦ���ֳ�������ֻ��һ�������Ͷȣ����Ժ��м����������ܷ���������Ӧ��ˮ�ⷴӦ��c��������ֻ��2��ȡ����������2��ȡ����Ϊ��OH�ͩ�CH2CH2��OCHO���ߩ�OH�ͩ�CH��CH3����OCHO�����ڱ����Ͽ������ڡ��䡢���γɻ�������������������ͬ���칹�干��6�֣�д�����б�����һ�ȴ��������ֵ�Ϊ��λ�ṹ���ṹ��ʽΪ��
��a����FeCl3��Һ��ɫ��˵�����з��ǻ���b���ܷ���������Ӧ��ˮ�ⷴӦ���ֳ�������ֻ��һ�������Ͷȣ����Ժ��м����������ܷ���������Ӧ��ˮ�ⷴӦ��c��������ֻ��2��ȡ����������2��ȡ����Ϊ��OH�ͩ�CH2CH2��OCHO���ߩ�OH�ͩ�CH��CH3����OCHO�����ڱ����Ͽ������ڡ��䡢���γɻ�������������������ͬ���칹�干��6�֣�д�����б�����һ�ȴ��������ֵ�Ϊ��λ�ṹ���ṹ��ʽΪ�� ��
��  �����Դ��ǣ�6��
�����Դ��ǣ�6��  ��
��  ��
��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ��CO��CO2�ǻ������糧�ͷų�����Ҫβ����Ϊ���ٶԻ�����ɵ�Ӱ�죬���糧��ͼ�������·���������Դ�����ã����»��ȼ�ϻ���Ҫ��ҵ��Ʒ��
(1)CO��Cl2�ڴ����������ºϳɹ���(COCl2)��ij�¶��£���2L���ܱ�������Ͷ��һ������CO��Cl2���ڴ����������·�����Ӧ��CO(g) +Cl2(g) ![]() COCl2(g) ����H = a kJ/mol��Ӧ�����вⶨ�IJ����������±�:
COCl2(g) ����H = a kJ/mol��Ӧ�����вⶨ�IJ����������±�:
t/min | n(CO)/mol | n(Cl2)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
�ٷ�Ӧ0~2minĩ��ƽ������v(COCl2)=______mol/(L��min)��
����2min~4min�䣬v��(Cl2) _________v��(CO) (����>������=������<��)�� ���¶���K = _____��
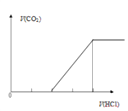
�� ��֪X��L�ɷֱ�����¶Ȼ�ѹǿ����ͼ��ʾLһ��ʱ��CO�� ת������X�ı仯��ϵ��
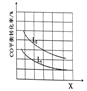
X�������������� __________��a_____ 0 (����>������=������<��)��
(2)�ڴ���������NO��COת��Ϊ�����壺 2CO(g)��2NO(g) ![]() 2CO2(g)��N2 (g) ����H=��748 kJ��mol-1
2CO2(g)��N2 (g) ����H=��748 kJ��mol-1
��һ�������£���λʱ���ڲ�ͬ�¶��²ⶨ�ĵ�������ת������ͼ1��ʾ���¶ȸ���710Kʱ�����¶ȵ����ߵ�������ת���ʽ��͵�ԭ������� ________________ ��
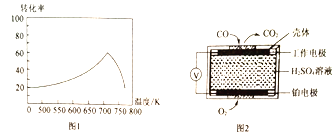
����֪���ⶨ������NO��CO �������õķ��������֣�����1���绯ѧ������������������CO�������Ĺ���ԭ����ͼ2��ʾ�������缫�ķ�ӦʽΪ________________������2��������ԭ�ζ�������H2O2��Һ����β��������������ת��Ϊǿ�ᣬ������к͵ζ����ⶨǿ�����ȡ�д��NO ��H2O2��Һ��Ӧ�����ӷ���ʽ��________________________________��
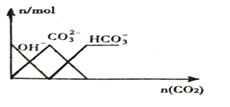
(3)NO2 ����Ⱦ����������Na2CO3 ��Һ����NO2 ������CO2����֪9.2g NO2�����Na2CO3 ��Һ��ȫ��Ӧʱת�Ƶ���0.1mol��ǡ�÷�Ӧ��ʹ����Һ�е�CO2��ȫ�ݳ���������Һ�������ԣ�����Һ�д��ڵ���������Ũ�ȴ�С��ϵ��_____________________��
����Ŀ�����й��ڴ��������ǿ����ʡ�������ʺͷǵ���ʵ���ȷ����ǣ�������
������ | ����� | ǿ����� | ������� | �ǵ���� | |
A | ���� | ���� | ̼�� | ��ˮ | ��ˮ |
B | ���� | ��� | ���Լ� | ������ | �ɱ� |
C | ʯ�� | ʯ��ʯ | ���� | ���� | ˮ |
D | �ռ� | ��Ȼ�� | �Ȼ��� | ̼���� | ���� |
A. A B. B C. C D. D