��Ŀ����
����Ŀ��NaClO��KAl(SO4)2������Ҫ�Ļ�����Ʒ������Ӧ������ֽҵ��
��1��NaClO��ҺpH��7�������ӷ���ʽ��ʾԭ��__________
��2������NaClO�������Ʋ⣬��ֽ���м���NaClO��Һ��Ŀ����_________________��
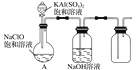
��3��ijС��ͬѧ����ͼ��ʾװ��̽������NaClO��KAl(SO4)2��Һ��Ϸ�Ӧ��ʵ�顣��������ƿ�м��뱥��KAl(SO4)2��Һ�����������İ�ɫ��״��������Ӧ�����ӷ���ʽ_____________��
���𰸡� ClO����H2O ![]() HClO��OH�� Ư��ֽ�� Al3����3ClO����3H2O===3HClO��Al(OH)3��
HClO��OH�� Ư��ֽ�� Al3����3ClO����3H2O===3HClO��Al(OH)3��
����������1��NaClO��ҺpH��7��ԭ���Ǵ���������ӻ�ˮ�⣬�������ӷ���ʽ��ʾΪ��ClO����H2O![]() HClO��OH����
HClO��OH����
��2��NaClO���ԺͿ����еĶ�����̼�������ɾ���Ư���Ե�HClO������ֽ���м���NaClO��Ŀ����Ϊ��Ư�ס�
��3��Al3+������ClO-����˫ˮ�ⷴӦ���õ����������İ�ɫ��״����������ʽΪ��Al3����3ClO����3H2O===3HClO��Al(OH)3����

��ϰ��ϵ�д�
 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д� ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
�����Ŀ