题目内容
【题目】流动电池是一种新型电池。其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O。下列说法正确的是
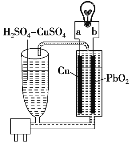
A.b为负极,a为正极
B.该电池工作时,内电路中电子由电极a流向电极b
C.b极的电极反应为PbO2 + 4H++4e-= Pb2++2H2O
D.调节电解质溶液的方法是补充H2SO4
【答案】D
【解析】
A.根据电池总反应为Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O,则Cu失电子发生氧化反应为负极,PbO2得电子发生还原反应为正极,所以为a负极,b为正极,A错误;
B.内电路是离子的定向移动,电子不能进入电解质溶液中,B错误;
C.PbO2得电子发生还原反应为正极,反应式为:PbO2+4H++SO42-+2e-=PbSO4+2H2O,C错误;
D.由电池总反应可知,则调节电解质溶液的方法是补充H2SO4,D正确;
故选D。

 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:
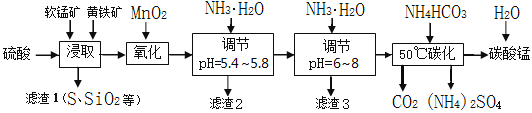
已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
金属离子 | Fe2+ | Fe3+ | Al3+ | Cu2+ | Mn2+ |
开始沉淀pH | 7.5 | 2.7 | 4.1 | 5.9 | 8.8 |
完全沉淀pH | 9.5 | 3.7 | 5.4 | 6.9 | 10.8 |
(1)提高浸出率的可采取的措施有_________。
A.适当升高温度 B.搅拌 C.加适量纯碱 D.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是____________________________________________。
(3)调节pH为5.4~5.8的目的是_____________________________________________。
(4)滤渣3的主要成分的化学式是_____________。
(5)50℃碳化过程发生反应的离子方程式是____________________________________。