题目内容
【题目】某有机物(分子式为C13H18O2)是一种食品香料,其合成路线如下图所示。

通过质谱法测得A的相对分子质量为56,它的核磁共振氢谱显示有两组峰且峰面积之比为1∶3;D分子中含有支链;F分子中含有苯环但无甲基,E可发生银镜反应,在催化剂存在下1molE与2 molH2可以发生反应生成F。请回答:
(1)A的化学名称为__________ ,B中所含官能团的名称为________,E的结构简式为________。
(2)C与新制Cu(OH)2悬浊液反应的离子方程式为________________________________。
(3)D与F反应的化学方程式为_______________________;其反应类型是_____________。
(4)写出符合下列条件的F的同分异构体_______________________________(写出其中的一种即可,F除外)
①遇FeCl3溶液显紫色;②核磁共振氢谱有四种不同化学环境的氢,且峰面积比为1:2:3:6。
(5)苯乙酸乙酯(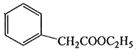 )是一种重要的医药中间体。写出以苯乙酮(
)是一种重要的医药中间体。写出以苯乙酮(![]() )和乙醇为主要原料制备苯乙酸乙酯的合成路线流程图(无机试剂任选)。
)和乙醇为主要原料制备苯乙酸乙酯的合成路线流程图(无机试剂任选)。
合成路线流程图请参考如下形式:
![]() __________________________________________________
__________________________________________________
【答案】 2-甲基丙烯 羟基 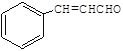
![]() + 2Cu(OH)2
+ 2Cu(OH)2![]()
![]() H+ Cu2O↓ +2H2O
H+ Cu2O↓ +2H2O ![]() +
+![]()
![]()
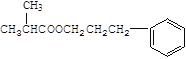 + H2O 取代(酯化)
+ H2O 取代(酯化) 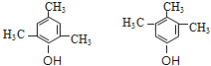
【解析】有机物A属于烃类,其相对分子质量为56,则![]() =4…8,可知A的分子式为C4H8,A发生信息中的反应生成B,B可以连续发生氧化反应,A的核磁共振氢谱有2组峰且峰面积之比为1:3,则A为(CH3)2C=CH2,B的结构简式为(CH3)2CHCH2OH,C的结构简式为(CH3)2CHCHO,D的结构简式为(CH3)2CHCOOH,D和F反应生成有机物C13H18O2,应是发生酯化反应,则F为醇,D中含有4个碳原子,所以F中含有9个碳原子,F的分子式为C9H12O,E可以发生银镜反应,含有-CHO,在催化剂存在条件下1mol E与2mol H2反应可以生成F,F分子中含有苯环但无甲基,可推知E为
=4…8,可知A的分子式为C4H8,A发生信息中的反应生成B,B可以连续发生氧化反应,A的核磁共振氢谱有2组峰且峰面积之比为1:3,则A为(CH3)2C=CH2,B的结构简式为(CH3)2CHCH2OH,C的结构简式为(CH3)2CHCHO,D的结构简式为(CH3)2CHCOOH,D和F反应生成有机物C13H18O2,应是发生酯化反应,则F为醇,D中含有4个碳原子,所以F中含有9个碳原子,F的分子式为C9H12O,E可以发生银镜反应,含有-CHO,在催化剂存在条件下1mol E与2mol H2反应可以生成F,F分子中含有苯环但无甲基,可推知E为![]() ,F为
,F为![]() ,则G为
,则G为![]() .
.
(1)A为(CH3)2C=CH2,其化学名称为2-甲基丙烯;B为(CH3)2CHCH2OH,含有的官能团为羟基;E的结构简式为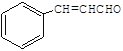 ;
;
(2)C为(CH3)2CHCHO,与新制Cu(OH)2悬浊液反应的化学方程式为:(CH3)2CHCHO+2Cu(OH)2+NaOH![]() (CH3)2CHCOONa+Cu2O↓+3H2O;
(CH3)2CHCOONa+Cu2O↓+3H2O;
(3)D+F→G的化学方程式: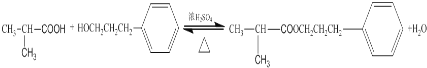 ,属于取代反应;
,属于取代反应;
(4)F(![]() )的同分异构体满足:①遇FeCl3溶液显紫色,说明含有酚羟基;②核磁共振氢谱有四种不同化学环境的氢,且峰面积比为1:2:3:6,符合条件的同分异构体为:
)的同分异构体满足:①遇FeCl3溶液显紫色,说明含有酚羟基;②核磁共振氢谱有四种不同化学环境的氢,且峰面积比为1:2:3:6,符合条件的同分异构体为: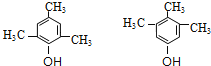 ;
;
(5)![]() 发生加成反应生成
发生加成反应生成![]() ,再发生消去反应生成
,再发生消去反应生成![]() ,经过B2H6、H2O2/OH-得到
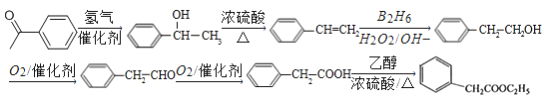
,经过B2H6、H2O2/OH-得到![]() ,氧化生成苯乙醛,进一步氧化生成苯乙酸,再与乙醇发生酯化反应生成苯乙酸乙酯,合成路线流程图为:
,氧化生成苯乙醛,进一步氧化生成苯乙酸,再与乙醇发生酯化反应生成苯乙酸乙酯,合成路线流程图为: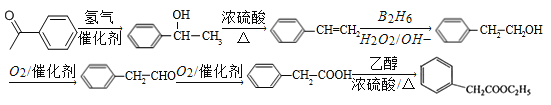 。
。


