题目内容
【题目】由铁、锌、铝、镁四种金属中的两种组成的混合物11 g,与足量的盐酸反应产生的氢气在标准状况下为11.2 L,则混合物中一定含有的金属是( )
A. 铁 B. 锌 C. 镁 D. 铝
【答案】D
【解析】标准状况下11.2L氢气的物质的量是0.5mol,需要金属的质量分别是:锌32.5g,铁28g,铝9g,镁12g,根据平均值思想,混合物中的两种金属需要量应分别小于和大于11g,而小于混合物11g的只有铝,因此一定含有铝,答案选D。

【题目】某同学想通过下图装置实验,探究 SO2 与 Na2O2反应的产物。
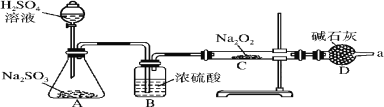
Ⅰ、检验反应中是否有 O2 生成的方法是_______________________________________;若有 O2 生成,请写出装置 C 中的化学方程式:________________________。
Ⅱ、A 中盛装 H2SO4 溶液的仪器名称是________;D 装置除起了防止空气中的水蒸气和二氧化碳进入 C 装置与 Na2O2 反应作用外,还可以________________________________。
Ⅲ、(1)C 中固体产物可能有三种情况:①只有 Na2SO3;②只有________;③Na2SO3 和 Na2SO4 混合物。
(2)若 Na2O2 反应完全,为确定 C 中固体产物的成分,该同学设计如下,请您利用限选试剂和仪器帮助他完成该探究过程。限选试剂和仪器:
0.01 mol·L-1 KMnO4酸性溶液 0.1 mol·L-1 Ba(NO3)2 溶液 0.1 mol·L BaCl2
1 mol·L-1 HNO3 溶液 1 mol·L-1 盐酸、试管、胶头滴管。
实验操作 | 预期现象和结论 |
步骤一:取少量 C 中固体产物 于试管中,加入适量的蒸馏水、 搅拌溶解,分别取少量于 A、B 试管中 | 固体完全溶解,得到无色透明溶液 |
步骤二:取试管 A,向溶液中 加入________________,振荡,观察溶液颜色变化 | __________________________ |
步骤三:取试管 B,向其中先 加入__________________ ,振 荡;再加入_______________,振荡 | 产生气泡 ,再加入 另一试剂看到产生白色沉淀, 则固体 C 中还含有________ |