题目内容
【题目】如图为几种晶体或晶胞的示意图:
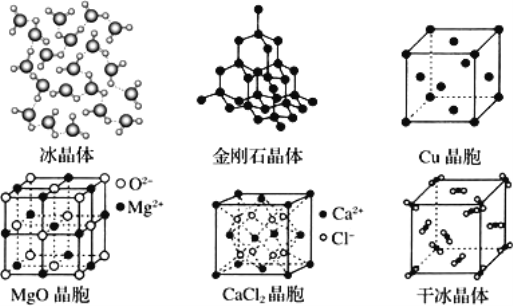
请回答下列问题:
(1)a:冰、b:金刚石、c:MgO、d:CaCl2、e:干冰 5 种晶体的熔点由高到低的顺序为________
(2)金刚石晶胞中若碳原子半径为 r,根据硬球接触模型,列式表示碳原子在晶胞中的空间占有率________(计算结果为含 π 的分数,不要化为小数或百分数)。
【答案】b>c>d>a>e ![]()
【解析】
(1)一般情况,原子晶体的熔点>离子晶体>分子晶体,金刚石是原子晶体,MgO和CaCl2是离子晶体,冰和干冰是分子晶体。对于MgO和CaCl2熔点比较,主要看晶格能,晶格能越大,熔点越高,离子半径越小,所带电荷越多,其晶格能越大,所以MgO熔点大于CaCl2;冰中水分子间又存在氢键,所以冰的熔点大于干冰,故答案为:b>c>d>a>e;
(2)金刚石晶胞可以表示为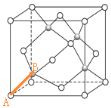 AB两个原子紧密相邻,AB两个原子中心的距离为半径的2倍,其长度为体对角线长度的
AB两个原子紧密相邻,AB两个原子中心的距离为半径的2倍,其长度为体对角线长度的![]() ,若晶胞的边长为a,则晶胞体对角线长度与四个碳原子直径相同,即
,若晶胞的边长为a,则晶胞体对角线长度与四个碳原子直径相同,即![]() a=8r,则a=
a=8r,则a=![]() r;根据均摊法该晶胞中碳原子的个数为
r;根据均摊法该晶胞中碳原子的个数为![]() =8,碳原子的体积为:8×
=8,碳原子的体积为:8×![]() ×πr3,晶胞体积为:a3=
×πr3,晶胞体积为:a3=![]() ,所以碳原子的空间利用率为:
,所以碳原子的空间利用率为: 。
。

【题目】Ⅰ.下表是元素周期表的一部分, 回答下列问题:
a | ||||||||
b | c | d | e | |||||
f | g | h | i |
(1)d、e、f对应简单离子的半径由大到小的顺序为_______(用具体微粒符号表示)。
(2)元素i的单质溶于水,生成一种具有漂白作用的化合物,该化合物的电子式为_____;写出a与c形成的一种含18电子且既含极性键又含非极性键的化合物的分子式_________。
(3)以元素a的单质为燃料,以f的最高价氧化物对应的水化物为电解质溶液,请写出该燃料电池的负极反应方程式_________。
Ⅱ. (1)根据下列信息判断氢气燃烧生成水时的热量变化:
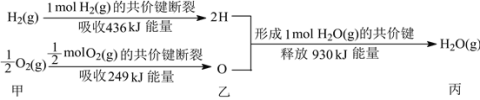
①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为________kJ;
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:________;
(2)铅蓄电池是最常见的二次电池,放电时的化学方程式为:Pb(s) + PbO2(s) + 2H2SO4(aq) = 2PbSO4(s) + 2H2O。负极反应式为__________,一段时间后,负极增重48克,转移电子_______mol。