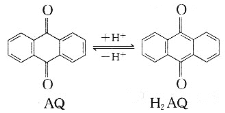
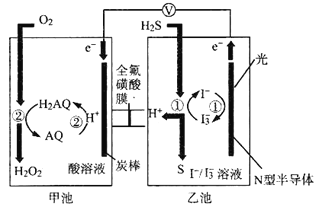
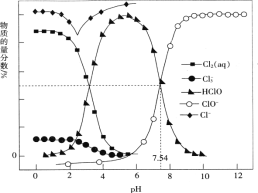
��Ŀ����
����Ŀ�����Բ��ϲ�ҵ��21���������չ�ĸ߿Ƽ�֧����ҵ֮һ����Ϊ��Ϣ��ҵ�ͻ��繤ҵ����Ҫ�������ܲ��ϣ����Բ��Ϲ㷺���ڵ�����Ϣ�����¼���������̼������Ҫ�����Ʊ����������壬��ҵ�������̿�(��Ҫ�ɷ�ΪMnO2)�ͻ�����(��Ҫ�ɷ�ΪFeS2)Ϊ��Ҫԭ���Ʊ�̼���̵���Ҫ�����������£�

��֪�����ֽ������ӳ�����pH���±���
Fe2�� | Fe3�� | Cu2�� | Mn2�� | |
��ʼ������pH | 7.5 | 3.2 | 5.2 | 8.8 |
��ȫ������pH | 9.2 | 3.7 | 7.8 | 10. 4 |
�ش��������⣺
��1��Ϊ������ܽ�������ԭ�ϵĽ���Ч�ʣ���ȡ�Ĵ�ʩ����������________��
A������ B���ʵ������¶� C����ĥ��ʯ D����������������ˮ
��2���ܽ���������Ҫ�����Ľ���������ΪFe3����Mn2������ȡ�����Һ�к�������Fe2����Cu2����Ca2�������ڼ���ʯ�ҵ�����Һ��pH�Ӷ�ʹ��Ԫ�ر���ȫ����ǰ���������������̿��䷢����Ӧ�����ӷ���ʽΪ____________________������ʯ�ҵ�����ҺpH�ķ�ΧΪ____________________��
��3�����������Ŀ���dz�ȥ��Һ�е�Cu2����Ca2�������ʣ���������Ҫ��________(�ѧʽ)��CaF2���������Һ��c(F��)Ϊ0.01mol��L��1������Һ�в���c(Ca2��)Ϊ________mol��L��1[��֪��Ksp(CaF2)��1.46��10��10]��
��4��������Ϊ����������ʹ��NaF��������Ⱦ��������(NH4)2CO3����NaF��������(NH4)2CO3����NaF��ȱ����______________________________________��
��5����ͼΪ������������������̽����ʵ�Ӱ�죬����ͼ����Ϣ�����������������Ӧ������________�����ҡ�
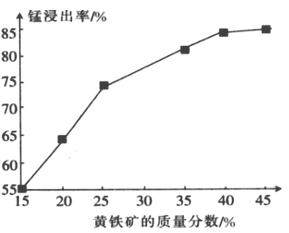
���𰸡�D MnO2��2Fe2����4H����2Fe3����Mn2����2H2O 3.7~5.2 CuS 1.46��10��6 ��ʹMn2��������������������̼���̵IJ��� 40
��������
�����̿�֪���̿���Ҫ�ɷ�MnO2���ͻ������������������˵õ�����Һ��������ҺpH��ʹ������ȫ�����������˵õ�����Һ����Ҫ����Cu2����Ca2�������ʣ��������ƺͷ����ƣ���ȥCu2����Ca2�����ˣ�����Һ�м���̼����狀Ͱ�ˮ���˵õ������Һ���ȸϳ������ᾧ�����õ�����泥�����Ϊ̼���̣�ͨ��ϴ�ӡ���ɵõ������̾��塣
��1�������¶ȡ����衢��С����Ŀ����Ⱦ��ܼ��ٹ�����ܽ⣬����Ϊ������ܽ�������ԭ�ϵĽ���Ч�ʣ����Բ�ȡ�Ĵ�ʩ�У��ʵ������¶ȣ����裬��ĥ��ʯ����ȡ�Ĵ�ʩ��������ΪD��
��2���������������̿�Ϊ�˽�������������Ϊ�����ӣ����ڳ�������ȥ���䷢����Ӧ�����ӷ���ʽΪ MnO2��2Fe2����4H����2Fe3����Mn2����2H2O�� �ɱ������ݿ�֪������������ȫ�ij�����pHΪ3.7��ͭ���ӿ�ʼ������pHΪ5.2�����Լ���ʯ�ҵ�����Һ��pH�ķ�ΧΪ3.7��5.2��
��3��������Ҫ��CuS��CaF2���������Һ��c(F��)Ϊ0.01mol��L��1������Һ�в���c(Ca2��)ΪKsp(CaF2)��c2(F��)=1.46��10��10��(0.01)2=1.46��10��6 mol��L��1��
��4��̼�������ܣ���(NH4)2CO3����NaF��ȱ���ǻ�ʹMn2��������������������̼���̵IJ��ʣ�
��5����ͼ�ɶ��������������������Ӧ������40������.