题目内容
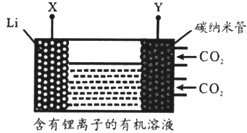
【题目】现有一种锂离子二次电池,其工作原理如图。放电时生 成的Li2CO3固体和碳储存于碳纳米管中。下列说法错误的是
A. 该电池中的有机溶剂不能含活性较大的氢
B. 充电时,Y为阳极,Li+向X电极移动
C. 放电时,负极反应为2Li+CO32-—2e-===Li2CO3
D. 放电时,电池总反应为3CO2+4Li===2Li2CO3+C
【答案】C
【解析】
A、锂是活泼金属;
B、充电时阳极发生氧化反应,Y为阳极,Li+向X电极移动;
C、放电时,负极反应为Li—e-=Li+;
D、放电时,锂作还原剂,二氧化碳作氧化剂,电池总反应为3CO2+4Li===2Li2CO3+C;
A、锂是活泼金属,该电池中的有机溶剂不能含活性较大的氢,否则锂会与有机溶剂发生反应,故A正确;
B、充电时阳极发生氧化反应,Y为阳极,Li+向阴极X电极移动,故B正确;
C、放电时,碳酸根离子不能通过有机溶剂,负极反应为Li—e-=Li+,故C错误;
D、放电时,锂作还原剂,二氧化碳作氧化剂,电池总反应为3CO2+4Li===2Li2CO3+C,故D正确;
故选C。

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案【题目】在100℃时,将0.200 mol的四氧化二氮气体充入2 L真空的密闭容器中,每隔一定的时间对该容器内的物质进行分析,得到如下表格:
时间s 浓度mol/L | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
(1)该反应达到平衡时,四氧化二氮的转化率为__________%,表中c2_____c3、a_____b(填“>”、“<”或“=”)。
(2)20s时四氧化二氮的浓度c1=_________mol/L,在0 s~20 s时间段内,四氧化二氮的平均反应速率为______________mol/(L·s)。
(3)100℃时,该反应的平衡常数K = ______________________
(4)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是_____________mol/L。
【题目】下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是

物质 选 项 | a | b | c |
A | Al | AlCl3 | Al(OH)3 |
B | CH3CH2OH | CH3CH2Br | CH3COOH |
C | CH3CH2OH | CH3COOH | CH3COOC2H5 |
D | CH3CH2Br | CH3CH2OH | CH3CHO |
A. A B. B C. C D. D