题目内容
【题目】我国芒硝(Na2SO4·10H2O)的储量丰富,它是重要的化工原料。
(1)制备碳酸钠。
①以芒硝和碳酸氢铵为原料,在水溶液中经复分解反应析出NaHCO3晶体,其反应的化学方程式是________。
②已知:ⅰ.2NaOH(s) + CO2(g) == Na2CO3(s) + H2O(g) ΔH1=127.4 kJ·mol 1
ⅱ.NaOH(s) + CO2(g) == NaHCO3(s) ΔH2=131.5 kJ·mol 1
反应2NaHCO3(s) == Na2CO3(s) + H2O(g) + CO2(g) ΔH= ________ kJ·mol 1。
(2)制备烧碱和硫酸。
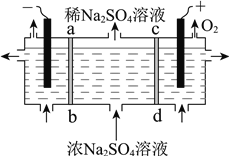
用右图所示装置,以惰性电极进行电解,ab、cd均为离子交换膜。则阳极区制备的溶液是________,阴极的电极反应式是________。
【答案】 Na2SO4 + 2NH4HCO3== 2NaHCO3↓+ (NH4)2SO4 +135.6 H2SO4溶液 2H+ + 2e– == H2↑或2H2O+ 2e– == H2↑+ 2OH
【解析】(1)①以芒硝和碳酸氢铵为原料,在水溶液中经复分解反应析出NaHCO3晶体,其反应的化学方程式是Na2SO4 + 2NH4HCO3== 2NaHCO3↓+ (NH4)2SO4。
②已知:ⅰ.2NaOH(s) + CO2(g) == Na2CO3(s) + H2O(g) ΔH1=127.4 kJ·mol 1
ⅱ.NaOH(s) + CO2(g) == NaHCO3(s) ΔH2=131.5 kJ·mol 1
由(ⅰ-ⅱ![]() )可得,2NaHCO3(s) == Na2CO3(s) + H2O(g) + CO2(g),所以该反应的ΔH=(127.4 kJ·mol 1)-(131.5 kJ·mol 1)
)可得,2NaHCO3(s) == Na2CO3(s) + H2O(g) + CO2(g),所以该反应的ΔH=(127.4 kJ·mol 1)-(131.5 kJ·mol 1)![]() +135.6 kJ·mol 1。
+135.6 kJ·mol 1。
(2)由图中信息可知,该装置左室为阴极室、右室为阳极室。因为电解后硫酸钠溶液浓度变小,所以电解过程中,硫酸根离子向阳极区移动、钠离子向阴极区移动。阳极氢氧根离子放电产生氧气,破坏了水的电离平衡,生成硫酸。阴极氢离子放电破坏了水的电离平衡生成氢氧化钠。综上所述,阳极区制备的溶液是H2SO4溶液,阴极的电极反应式是2H+ + 2e– == H2↑或2H2O+ 2e– == H2↑+ 2OH。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】在10 L密闭容器中充入气体X和Y,发生反应X(g) + Y(g)![]() M(g) + N(g) ΔH,所得实验数据如下表:
M(g) + N(g) ΔH,所得实验数据如下表:
实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.40 | 0.10 | 0.090 |
② | 800 | 0.40 | 0.10 | 0.080 |
③ | 800 | 0.20 | 0.05 | a |
下列说法正确的是
A. ①中,若5 min末测得n (M)=0.050 mol,则0至5 min内,用N表示的平均反应速率υ (N)=1.0×10 2 mol/(L·min)
B. 800 ℃,该反应的平衡常数K=2.0
C. ③中,达到平衡时,Y的转化率为80%
D. ΔH>0
【题目】甲醇是重要的化工原料,发展前景广阔。
(1)利用甲醇可制成微生物燃料电池(利用微生物将化学能直接转化成电能的装置)。某微生物燃料电池装置如右图所示:A极是________极(填“正”或“负”),其电极反应式是________。

(2)研究表明CO2加氢可以合成甲醇。CO2和H2可发生如下两个反应:
I.CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) ΔH1
CH3OH(g) + H2O(g) ΔH1
II.CO2(g) + H2(g)![]() CO(g) + H2O(g) ΔH2
CO(g) + H2O(g) ΔH2
①反应I的化学平衡常数表达式K=________。
②有利于提高反应I中 CO2的平衡转化率的措施有________(填序号)。
a.使用催化剂 b.加压 c.增大CO2和H2的初始投料比
③研究温度对于甲醇产率的影响。在210 ℃~290 ℃,保持原料气中CO2和H2的投料比不变,按一定流速通过催化剂甲,主要发生反应I,得到甲醇的实际产率、平衡产率与温度的关系如右图所示。

ΔH1________0(填“>”、“=”或“<”),其依据是________。
④某实验控制压强一定,CO2和H2初始投料比一定,按一定流速通过催化剂乙,经过相同时间测得如下实验数据(反应未达到平衡状态):
T(K) | CO2实际转化率(%) | 甲醇选择性(%)【注】 |
543 | 12.3 | 42.3 |
553 | 15.3 | 39.1 |
【注】甲醇选择性:转化的CO2中生成甲醇的百分比
表中实验数据表明,升高温度,CO2的实际转化率提高而甲醇的选择性降低,其原因是________。
