题目内容
食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的。已知:
氧化性:IO3->Fe3+>I2;还原性:S2O32->I-
3I2+6OH-=5I-+IO3-+3H2O
KI+I2 KI3
KI3
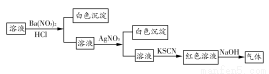
(1)某学习小组对加碘盐进行了如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得试液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①加KSCN溶液显红色,该红色物质是 (用化学式表示);CCl4中显紫红色的物质是 (用电子式表示)。
②第二份试液中加入足量KI固体后,反应的离子方程式为 、 。
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境中KI与氧气反应的化学方程式: 。
将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质作为食盐加碘剂是否合适? (填“是”或“否”),并说明理由: 。
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的是 。
A.Na2S2O3 B.AlCl3
C.Na2CO3 D.NaNO2
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂。请设计实验方案,检验该加碘盐中的Fe2+:
(1)①Fe(SCN)3 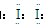
②IO3-+5I-+6H+=3I2+3H2O 2Fe3++2I-=2Fe2++I2
(2)O2+4KI+2H2O=2I2+4KOH 否
KI3在受热(或潮湿)条件下产生I2和KI,KI易被氧气氧化,I2易升华
(3)AC
(4)取足量该加碘盐溶于蒸馏水中,用盐酸酸化,滴加适量氧化剂(如:氯水、过氧化氢等),再滴加KSCN溶液,若显血红色,则该加碘盐中存在Fe2+
【解析】(1)①加KSCN溶液后显红色,发生的反应为:Fe3++3SCN-=Fe(SCN)3,红色物质是Fe(SCN)3;CCl4中显紫红色的物质是I2,其电子式为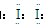 。
。
②由(1)中信息可知,加碘盐中含有Fe3+和IO3-,试液中加入足量KI固体后,发生的离子反应为:IO3-+5I-+6H+=3I2+3H2O,2Fe3++2I-=2Fe2++I2。
(2)KI具有还原性,在潮湿的环境中与O2发生氧化还原反应:O2+4KI+2H2O=2I2+4KOH。由题中信息可知,KI3·H2O在受热(或潮湿)的条件下发生反应KI3??KI+I2,而KI易被氧气氧化为I2,而I2受热易升华,从而引起碘的损失,故KI3·H2O不适合做食盐加碘剂。
(3)由于还原性:S2O32->I-,故加Na2S2O3可减少KI被氧化;由3I2+6OH-=5I-+IO3-+3H2O可知,I-在碱性条件下不易被氧化为I2,故加入Na2CO3也可减少KI被氧化,故Na2S2O3、Na2CO3均可作稳定剂。
(4)取足量该加碘盐溶于蒸馏水中,用盐酸酸化,滴加适量氯水或过氧化氢等氧化剂,再滴加KSCN溶液,若显血红色,则该加碘盐中存在Fe2+,涉及的反应有:2Fe2++Cl2=2Fe3++2Cl-或2Fe2++H2O2+2H+=2Fe3++2H2O,Fe3++3SCN-=Fe(SCN)3。