题目内容
【题目】已知漂白粉与浓盐酸反应可产生氯气,某同学试图测定氯气的体积并验证干燥纯净的氯气无漂白性,现有如下装置,请回答:
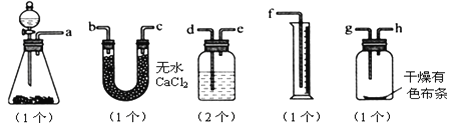
(1)请用字母填写装置的连接顺序:
a 接( ),( )接( ),( )接( ),( )接( ),( )接( )。
(2)洗气瓶中所装液体是 。
(3)在制氯气前,必须进行的一项操作步骤是 。
(4)某同学实验时,发现量筒中未收集到液体,则失败的原因可能是 。
(5)写出漂白粉与浓盐酸反应制氯气的化学方程式 。
【答案】(1)(d)(e);(b 或 c);(c 或 b);(g);(h)(e);(d);(f);
(2)饱和食盐水;(3)检查装置的气密性;
(4)盐酸浓度小,反应没发生;装置漏气;e 与 f 连接.
(5)Ca(ClO)2+4HCl=CaCl2+2Cl2↑+2H2O
【解析】
试题分析:(1)本实验有两个目的,其一是验证干燥的氯气没有漂白性;其二是测量氯气的体积,由于测量氯气的体积是根据排入量筒里的水来读出,所以验证干燥的氯气无漂白性的实验必须放在测量氯气的体积之前,所以其连接顺序为:发生装置→除氯化氢装置→除水蒸气→验证漂白性→排液体→收集液体,除去水蒸气可以用装有无水CaCl2的U型管,也可以用盛有浓硫酸的洗气瓶,则连接顺序是(d)(e);(b 或 c);(c 或 b);(g);(h)(e);(d);(f);。
(2)Cl2在饱和食盐水中的溶解度小(有时也用水代替),可除去Cl2中混有的HCl,所以洗气瓶中所装液体为饱和食盐水。
(3)任何气体的制备实验开始之前,都必须检查装置的气密性。
(4)最后由量筒和洗气瓶组成的“量气装置”,可以粗略地测定Cl2的体积,若量筒中未收集到液体,则失败的原因可能是盐酸浓度小,反应没发生;装置漏气;e 与 f 连接。
(5)漂白粉的主要成分是CaCl2和Ca(ClO)2,Ca(ClO)2与浓盐酸反应生成氯气、CaCl2和水,反应的化学方程式为Ca(ClO)2+4HCl=CaCl2+2Cl2↑+2H2O。

【题目】下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
叙述I | 叙述II | |
A | 氯气具有强还原性 | 可用于自来水的消毒杀菌 |
B | SiO2导电能力强 | 可用于制造太阳能电池板 |
C | SO2有还原性 | SO2能使酸性KMnO4溶液褪色 |
D | 盐酸和氨水都能溶解Al(OH)3 | Al(OH)3是两性氢氧化物 |