题目内容
【题目】某有机物是药物生产的中间体,其结构简式如图。下列有关叙述正确的是( )

A. 该有机物能与溴水发生加成反应
B. 该有机物与浓硫酸混合加热可发生消去反应
C. 1 mol 该有机物与足量NaOH溶液反应最多消耗3 mol NaOH
D. 该有机物经催化氧化后能发生银镜反应
【答案】D
【解析】试题分析:A、不含碳碳不饱和键,因此不能和溴水发生加成反应,故错误;B、醇羟基所连碳原子的相邻碳原子上不含氢原子,因此在浓硫酸加热时,不发生消去反应,故错误;C、1mol该物质含有1mol酚羟基和1mol氯原子、1mol的“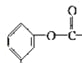 ”,因此消耗NaOH的物质的量为4mol,故错误;D、含有-CH2OH,能被氧化成-CHO,能和银氨溶液发生氧化反应,故正确。
”,因此消耗NaOH的物质的量为4mol,故错误;D、含有-CH2OH,能被氧化成-CHO,能和银氨溶液发生氧化反应,故正确。

【题目】

(1)该浓盐酸中HCl的物质的量浓度为__________mol·L-1。
(2)某学生欲用该浓盐酸和蒸馏水配制成1mol·L-1的稀盐酸。现实验室仅需要这种盐酸220mL,试回答下列问题:
①经计算需要______mL浓盐酸,在量取时宜选用下列量筒中的______。
A.5mL |
B.10mL |
C.25mL |
D.50mL |
②在量取浓盐酸后,进行了下列操作:
a等稀释的盐酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
b往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
c在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
d用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)____________。若量取的是浓硫酸,简述第c步实验的操作过程。
③在上述配制过程中,用量筒量取浓盐酸时仰视观察凹液面,其配制的稀盐酸浓度________(填“偏高”、“偏低”或“无影响”,下同)。若定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线,则配制的稀盐酸浓度________