题目内容
【题目】某一定量的苯的同系物A完全燃烧,生成的气体通过浓硫酸后,浓硫酸增重5.4克,再通过KOH溶液后,KOH溶液增重19.8克,(设浓硫酸和KOH溶液的吸收率为100%)。
(1)通过计算确定A的分子式。(写出计算过程)_________________
(2)若0.1molA的氧化产物(被酸性高锰酸钾氧化)恰好被2mol/L100mL的NaOH溶液完全中和。写出A可能的的结构简式。_________________________
(3)若A的核磁共振氢谱中只有2种峰,则写出A的结构简式。_____________________
【答案】 C9H12 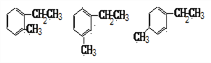

【解析】(1)设A的分子式为CnH2n-6。浓硫酸具有吸水性,增重5.4g为水的质量,物质的量是5.4g÷18g/mol=0.3mol,则n(H)=2n(H2O)=2×0.3mol=0.6mol,生成物通入KOH溶液,增重的19.8g质量为二氧化碳的质量,则n(CO2)=19.8g÷44g/mol=0.45mol,n(C)=n(CO2)=0.45mol,因此![]() ,解得n=9,所以该烃的分子式为C9H12;(2)若0.1molA的氧化产物(被酸性高锰酸钾氧化)恰好被2mol/L 100mL的NaOH溶液完全中和,氢氧化钠是0.2mol,这说明有两个烷基被高锰酸钾氧化转化为羧基,为甲乙苯,有邻间对三种,故结构简式为
,解得n=9,所以该烃的分子式为C9H12;(2)若0.1molA的氧化产物(被酸性高锰酸钾氧化)恰好被2mol/L 100mL的NaOH溶液完全中和,氢氧化钠是0.2mol,这说明有两个烷基被高锰酸钾氧化转化为羧基,为甲乙苯,有邻间对三种,故结构简式为 ;(3)若A的核磁共振氢谱中只有2种峰,则有两种氢,为均三甲苯,结构简式为
;(3)若A的核磁共振氢谱中只有2种峰,则有两种氢,为均三甲苯,结构简式为![]() 。
。

练习册系列答案
相关题目