题目内容
用如下装置可以完成一系列实验(图中夹持装置已略去)。
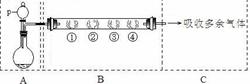
请回答下列问题:
Ⅰ.若用装置A选用浓硫酸和亚硫酸钠固体制取SO2气体(根据需要可以加热),并通过装置B完成表中设计实验,请填写表中空白:
II.若用装置A选用浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做了如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊溶液、④蘸有浓NaOH溶液。回答下列问题:
(1)p中盛装试剂为 。
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式 。①处包有的某固体物质可能是 。
a.MnO2 b.KMnO4 c.KCl d.Cu
(3)在整个实验过程中,在③处能观察到 。
(4)反应较长时间后,②处有棕黄色褪去,生成无色的IO3-,写出该反应的离子方程式: 。

请回答下列问题:
Ⅰ.若用装置A选用浓硫酸和亚硫酸钠固体制取SO2气体(根据需要可以加热),并通过装置B完成表中设计实验,请填写表中空白:
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | | | 褪色 | 浅黄色 |
| 体现SO2的性质 | | | | |
II.若用装置A选用浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做了如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊溶液、④蘸有浓NaOH溶液。回答下列问题:
(1)p中盛装试剂为 。
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式 。①处包有的某固体物质可能是 。
a.MnO2 b.KMnO4 c.KCl d.Cu
(3)在整个实验过程中,在③处能观察到 。
(4)反应较长时间后,②处有棕黄色褪去,生成无色的IO3-,写出该反应的离子方程式: 。
.I-----------------------------------------6分
II(1)浓硫酸---------------------------- ------------------------1分
------------------------1分
(2)Cl2 + 2I- = 2Cl- + I2 b-----------------------------------2分
(3)先变红后褪色--- -----------------------------------------1分
-----------------------------------------1分
(4)5Cl2 + I2 + 6H2O = 12H+ + 2IO3- + 10Cl----------------------------2分
| | | | | |
| | | | | |
| | 溶液变红 | 溶液褪色 | | |
| | 水溶液显酸性 | 漂白性 | 还原性 | 氧化性 |
 ------------------------1分
------------------------1分(2)Cl2 + 2I- = 2Cl- + I2 b-----------------------------------2分
(3)先变红后褪色---
 -----------------------------------------1分
-----------------------------------------1分(4)5Cl2 + I2 + 6H2O = 12H+ + 2IO3- + 10Cl----------------------------2分
略

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 Fe2O3+SO2↑+SO3↑+14H2O↑;下图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:
Fe2O3+SO2↑+SO3↑+14H2O↑;下图的装置可用来检验上述反应中所有的气体产物,请回答下列问题: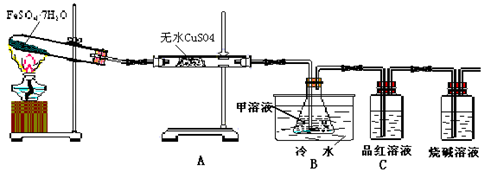
 形成一段水柱
形成一段水柱