题目内容
A、B、C、D是四种短周期元素,它们的相关信息如下表:
(1)表中所述A的单质晶体中微粒间的相互作用有______、______.
(2)B元素原子核外最外层电子的轨道表示式为______,其最高价氧化物对应水化物的化学特性是______.
(3)C元素的氢化物的分子为______ (填“极性“或”非极性“)分子,其溶于水后溶液呈碱性的原因是______(用方程式表示).
(4)与D同主族的短周期元素,其单质及其化合物与D的单质及化合物均具有的性质为______ (填序号).
A.一定条件下其单质易与活泼金属反应 B.气态氢化物极易溶于水并呈强酸性
C.气态氢化物具有很好的热稳定性 D.常温下单质跟水剧烈反应并放出氧气.
| 元素 | 元素性质及相关信息 |
| A | 其单质的一种晶体虽不是金属晶体,但是电的良导体,且难熔、质软并有润滑性,可作高温轴承的润滑剂、火箭发动机喷管和电极材料. |
| B | 其单质能与强酸、强碱溶液反应,其离子在第三周期单核阳离子中半径最小. |
| C | 是蛋白质的组成元素之一,原子核外有3种不同能量的电子,且未成对电子数最多. |
| D | 原子核外最外层电子排布为nsnnp2n+1. |
(2)B元素原子核外最外层电子的轨道表示式为______,其最高价氧化物对应水化物的化学特性是______.
(3)C元素的氢化物的分子为______ (填“极性“或”非极性“)分子,其溶于水后溶液呈碱性的原因是______(用方程式表示).
(4)与D同主族的短周期元素,其单质及其化合物与D的单质及化合物均具有的性质为______ (填序号).
A.一定条件下其单质易与活泼金属反应 B.气态氢化物极易溶于水并呈强酸性
C.气态氢化物具有很好的热稳定性 D.常温下单质跟水剧烈反应并放出氧气.
A、B、C、D是四种短周期元素.A元素单质的一种晶体虽不是金属晶体,但是电的良导体,且难熔、质软并有润滑性,可作高温轴承的润滑剂、火箭发动机喷管和电极材料,则A为碳元素.B元素单质能与强酸、强碱溶液反应,其离子在第三周期单核阳离子中半径最小,则B为铝元素.C元素是蛋白质的组成元素之一,原子核外有3种不同能量的电子,且未成对电子数最多,则C为氮元素.D元素原子核外最外层电子排布为nsnnp2n+1,s能级容纳2个电子,所以D元素原子核外最外层电子排布为2s22p5,则D为氟元素.
故A为碳元素,B为铝元素,C为氮元素,D为氟元素.
(1)表中所述A的单质为石墨,石墨为层状结构,层与层之间通过范德华力结合,层内碳原子之间形成共价键,石墨晶体中微粒间的相互作用有范德华力、共价键,
故答案为:共价键;范德华力;
(2)B为铝元素,原子核外最外层电子排布为3s23p1,轨道表示式为
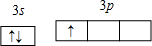
,其最高价氧化物对应水化物为氢氧化铝,化学特性是两性氧化物(即能与酸反应,又能与碱反应),
故答案为:

;两性氧化物(即能与酸反应,又能与碱反应);
(3)C元素的氢化物为NH3,空间结构为三角锥型,是极性分子,其溶于水后溶液呈碱性的原因是氨气与化合生成一水合氨,一水合氨电离出氢氧根离子,使溶液呈碱性,方程式为NH3+H2O

NH 3?H2O

NH4++OH-,故答案为:NH3+H2O

NH 3?H2O

NH4++OH-;
(4)D为氟元素,与D同主族的短周期元素为氯元素.
A.氟气、氯气具有强氧化性,一定条件下其单质易与活泼金属反应,故A正确;
B.氢氟酸是弱酸,氢氯酸是强酸,故B错误;
C.氟元素、氯元素的非金属性很强,气态氢化物具有很好的热稳定性,故C正确;
D.常温下氟气与水剧烈反应生成氧气,氯气与水反应不剧烈,不能生成氧气,故D错误.
故选AC.
故A为碳元素,B为铝元素,C为氮元素,D为氟元素.
(1)表中所述A的单质为石墨,石墨为层状结构,层与层之间通过范德华力结合,层内碳原子之间形成共价键,石墨晶体中微粒间的相互作用有范德华力、共价键,
故答案为:共价键;范德华力;
(2)B为铝元素,原子核外最外层电子排布为3s23p1,轨道表示式为

,其最高价氧化物对应水化物为氢氧化铝,化学特性是两性氧化物(即能与酸反应,又能与碱反应),
故答案为:

;两性氧化物(即能与酸反应,又能与碱反应);
(3)C元素的氢化物为NH3,空间结构为三角锥型,是极性分子,其溶于水后溶液呈碱性的原因是氨气与化合生成一水合氨,一水合氨电离出氢氧根离子,使溶液呈碱性,方程式为NH3+H2O

NH 3?H2O

NH4++OH-,故答案为:NH3+H2O

NH 3?H2O

NH4++OH-;
(4)D为氟元素,与D同主族的短周期元素为氯元素.
A.氟气、氯气具有强氧化性,一定条件下其单质易与活泼金属反应,故A正确;
B.氢氟酸是弱酸,氢氯酸是强酸,故B错误;
C.氟元素、氯元素的非金属性很强,气态氢化物具有很好的热稳定性,故C正确;
D.常温下氟气与水剧烈反应生成氧气,氯气与水反应不剧烈,不能生成氧气,故D错误.
故选AC.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
a、b、c、d是四种短周期元素.a、b、d同周期,c、d同主族.a的原子结构示意图为 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为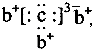 下列比较中正确的是( )
下列比较中正确的是( )
 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为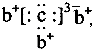 下列比较中正确的是( )
下列比较中正确的是( )| A、原子半径:a>c>d>b | B、最高价含氧酸的酸性c>d>a | C、原子序数:a>d>b>c | D、单质的氧化性a>b>d>c |
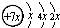 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
 Al(OH)3+OH-
Al(OH)3+OH-