题目内容
【题目】铁是人体必需元素,是合成血红素的重要原料,缺铁会造成贫血,市场上常见补血剂有硫酸亚铁、富马酸亚铁(分子式C4H2O4Fe)、葡萄糖酸亚铁、琥珀酸亚铁(速力菲片)等。某化学兴趣小组通过实验对硫酸亚铁补血剂成分进行探究并测定Fe2+的含量,可供选择的试剂有双氧水、KSCN溶液、盐酸、BaCl2溶液(已知KSCN可被双氧水氧化)。
(1)成分探究:小组成员发现硫酸亚铁补血剂外面糖衣是红色的,里面是淡蓝绿色的,甲同学对其组成进行如下探究:
实验探究 | 实验操作及现象 | 结论分析 |
探究一 | 将淡蓝绿色粉末溶解于盐酸溶液中,取上清液2份, ①1份滴加BaCl2溶液,产生白色沉淀,再加盐酸,无明显变化。 ②另1份溶液先滴加KSCN溶液,无明显变化,再滴加双氧水,后滴加___溶液,变成血红色。 | 证明淡蓝绿色粉末为FeSO4 |
探究二 | 将红色物质研成粉末,滴加盐酸,无明显变化,再滴加KSCN溶液,无明显现象。 | 证明:红色物质不是Fe2O3 |
(2)配制硫酸亚铁补血剂的待测溶液。
①补血剂(1片0.5克)![]() 浊液
浊液![]() 滤液
滤液![]() 配成1L待测液
配成1L待测液
步骤③浊液脱色后进行___(填标号)操作才能得到溶液。
A. B.
B.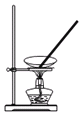
C.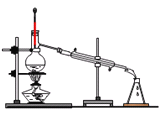 D.
D.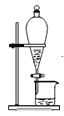
②甲同学认为步骤③滤液直接蒸发结晶不能得到硫酸亚铁晶体,理由是___,你的方案是___。
③已知步骤④中加入足量的H2O2溶液,作用是___,然后微热并用玻璃棒搅拌至无气泡产生,目的是___。
④写出步骤④中发生反应的离子方程式:___。
(3)测定硫酸亚铁补血剂待测液的浓度
方法一:用紫外分光光度法:使用紫外分光光度计,将不同波长的光连续地照射到一定标准浓度滴加5mL0.2molL-1苯二甲酸氢钾缓冲液的硫酸亚铁标准溶液,得到与不同波长相对应的吸收强度,以硫酸亚铁标准溶液的浓度为横坐标,吸光度为纵坐标,绘出该物质的吸收光谱曲线如图。
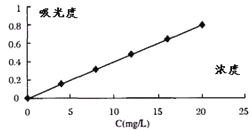
⑤取待测液10mL滴加5mL0.2molL-1苯二甲酸氢钾缓冲液,并稀释至60mL,用紫外分光光度法测得待测液的吸光度为0.4,则样品中铁元素的质量分数是___。
方法二:KMnO4标准溶液滴定法:称取4.0g的硫酸亚铁产品,溶于水,加入适量稀硫酸,用0.2molL-1KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液体积10.00mL。
⑥KMnO4溶液置于___式滴定管中,终点的颜色变化:___。
⑦要达到好的治疗效果,服用补血剂时需注意口服铁剂应同时并服维生素C,理由是 ___。
【答案】KSCN溶液 A 因为硫酸亚铁在加热过程中易被氧化 加入足量铁粉,小心蒸发至出现结晶膜时停止加热 将Fe2+完全氧化成Fe3+ 除去过量的H2O2 2Fe2++H2O2+2H+=2Fe3++2H2O 12% 酸 浅绿色变成浅黄色 维生素C具有还原性,防止Fe2+被氧化
【解析】
(1)②H2O2具有强氧化性,能将Fe2+氧化为Fe3+,检验Fe3+用KSCN溶液;
(2)①补血剂溶解得到浊液过滤后可得滤液;
②亚铁离子具有还原性,硫酸亚铁在加热过程中易被氧化;
③步骤④中加入足量的H2O2氧化亚铁离子为铁离子发生反应2Fe2++H2O2+2H+=2Fe3++2H2O;
④亚铁离子酸性溶液中钡过氧化氢氧化生成铁离子;
(3)⑤根据吸光度计算硫酸亚铁的浓度,将样品10ml稀释至60ml,可得原溶液硫酸亚铁的浓度,进一步可计算铁元素的质量分数;
⑥锰酸钾溶液具有强氧化性能氧化橡胶管,不能用碱式滴定管盛放,滴定终点时,溶液由浅绿色溶液变为黄色溶液;
⑦维生素C有还原性,可将铁离子还原成亚铁离子。
(1)②证明淡蓝绿色粉末为FeSO4,将淡蓝绿色粉末溶解于盐酸溶液中取上清液2份,加入氯化钡溶液生成不溶于盐酸的白色沉淀证明含硫酸根离子,另一份加入KSCN溶液无红色出现,加入过氧化氢,滴入KSCN溶液会变红色证明原溶液中为亚铁离子;
(2)①补血剂(1片0.5克)溶解得到浊液脱色后过滤得到滤液,
②滤液直接蒸发结晶不能得到硫酸亚铁晶体,因为亚铁离子具有还原性,硫酸亚铁在加热过程中易被氧化,在加热蒸发过程中应加入足量铁粉,小心蒸发至出现结晶膜时停止加热;
③步骤④中加入足量的H2O2溶液是为了氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,微热并用玻璃棒搅拌至无气泡产生除去过量的H2O2;
④亚铁离子酸性溶液中钡过氧化氢氧化生成铁离子,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(3)⑤吸光度为0.4,求得硫酸亚铁的浓度为10mg/L,样品10ml稀释至60ml,所以原溶液硫酸亚铁的浓度为60mg/L,0.5g样品含有硫酸亚铁60mg,进一步计算铁元素的质量分数![]() =12%;
=12%;
⑥锰酸钾溶液具有强氧化性能氧化橡胶管,不能用碱式滴定管盛放,应用酸式滴定管盛放,终点的颜色变化是浅绿色溶液变化为黄色溶液;
⑦维生素C有还原性,能服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于人体吸收。

【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
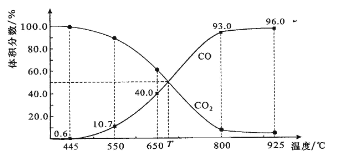
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为__(写离子符号);若所得溶液c(HCO3):c(CO32)=2:1,溶液pH=__。(室温下,H2CO3的K1=4×107;K2=5×1011)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
已知上述反应中相关的化学键键能数据如下:
化学键 | C—H | C=O | H—H | C |
键能/kJ·mol1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=__。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是__(填“A”或“B”)。
(3)向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)![]() CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①下列叙述能说明此反应达到平衡状态的是___。
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H-H键断裂
②产物甲醇可以用作燃料电池,碱性条件下的甲醇(CH3OH)燃料电池负极反应式:__。
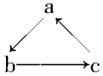
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是 ( )
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuSO4 | |
c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
A. AB. BC. CD. D