题目内容
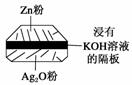
微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-。下列叙述正确的是( )
A.在使用过程中,电解质KOH被不断消耗
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.每转移2mol e-,有232gAg2O被氧化
D.Zn是负极,Ag2O是正极
D

常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,
两种溶液的物质的量浓度和混合溶液的pH如表所示:
| 实验编号 | HA的物质的量浓度(mol·L-1) | NaOH的物质的量浓度(mol·L-1) | 混合后溶 液的pH |
| 甲 | 0.1 | 0.1 | pH=7 |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,判断HA是 (填“强酸”或“弱酸”)
某同学欲利用甲组中的一元酸HA溶液滴定未知浓度的NaOH溶液,可选取 作指示剂;在滴定过程中,下列哪些操作会使结果偏高的是
A.酸式滴定管未用标准酸HA润洗,直接装入标准酸HA
B.酸式滴定管滴定前有气泡,滴定后气泡消失
C.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥
D.读取酸HA体积开始时仰视读数,滴定结束后俯视读数
E.锥形瓶用蒸馏水洗净后,再用待测NaOH溶液润洗
(2)根据乙组数据分析,乙组混合溶液中离子浓度c(A-)和c(Na+)的大小关系是
A.前者大 B.后者大 C.两者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是
(4)分析丁组数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)-c(A-)= mol·L-1。
某同学取丁组试剂各100mL,充分反应后测得放出的热量为Q,写出表示中和热的热化学方程式
 2H2O
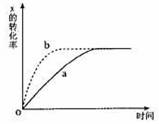
2H2O Z(g)+M(g) △H<0进行过程中X的转化
Z(g)+M(g) △H<0进行过程中X的转化