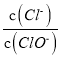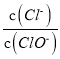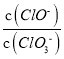题目内容
【题目】硅单质及其化合物应用范围很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
![]()
①写出由石英砂和焦炭在高温下制备粗硅的化学反应方程式:_____________。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种气体,写出配平的化学反应方程式: _____________;H2还原SiHCl3过程中若混入O2,可能引起的后果是______________。
(2)下列有关硅材料的说法正确的是_____________ (填字母代号)。
A.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
B.石英坩埚耐高温性强,可用于加热熔融氢氧化钠
C.神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料单晶硅也可以制作电脑芯片
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E.盐酸可以与硅反应,故可采用盐酸为抛光液抛光单晶硅
F.玛瑙饰品的主要成分与建筑材料砂子相同
【答案】 SiO2+2C![]() Si+2CO↑ SiHCl3+3H2O=H2SiO3↓+3HCl↑+H2↑ 氧气与氢气混合,可能引起爆炸,氧气可能会氧化SiHCl3 ACF
Si+2CO↑ SiHCl3+3H2O=H2SiO3↓+3HCl↑+H2↑ 氧气与氢气混合,可能引起爆炸,氧气可能会氧化SiHCl3 ACF
【解析】(1)①氢气和纯SiHCl3反应生成高纯硅和氯化氢:SiHCl3+H2![]() Si+3HCl,故答案为:SiHCl3+H2
Si+3HCl,故答案为:SiHCl3+H2![]() Si+3HCl;
Si+3HCl;
②SiHCl3遇水剧烈反应生成H2SiO3、HCl和氢气:SiHCl3+3H2O═H2SiO3+H2↑+3HCl,氢气遇氧气易爆炸,故答案为:SiHCl3+3H2O═H2SiO3↓+H2↑+3HCl↑;氧气与氢气混合,可能引起爆炸,氧气也可能会氧化SiHCl3;
(2)A.Si3N4均为原子晶体,熔点高,性质稳定,可用于制作高温陶瓷和轴承,故A正确; B.石英坩埚的主要成分为二氧化硅,二氧化硅能够与氢氧化钠反应,故B错误;C.硅是常见的半导体材料,可以制作电脑芯片和太阳能电池板,故C正确;D.玻璃是由纯碱、石灰石和石英制成的,玻璃属于混合物,没有固定的熔点,故D错误;E. 常温下,Si只能与唯一一种酸HF反应,不与HCl反应,故E错误;F.玛瑙和砂子的主要成分都是二氧化硅,故F正确;故答案为:ACF。

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案