��Ŀ����
2�� �⻯�ƣ�CaH2���Ƕ��ֳ��õĴ�����ϣ�Ҳ�ǵ�ɽ�˶�Ա���õ���Դ�ṩ������Ҫ�ܷⱣ�棬��ˮ��Ӧ�����������ƺ�������•ij�о���ѧϰС��ģ��������ҵ��ȡ�⻯��
�⻯�ƣ�CaH2���Ƕ��ֳ��õĴ�����ϣ�Ҳ�ǵ�ɽ�˶�Ա���õ���Դ�ṩ������Ҫ�ܷⱣ�棬��ˮ��Ӧ�����������ƺ�������•ij�о���ѧϰС��ģ��������ҵ��ȡ�⻯����ʵ�顿
��п����ϡ���ᷴӦ�Ƶø������������������������ڼ��ȵ�������ֱ�ӻ��ϣ������Ƶ�CaH2��
��1�������йظ�ʵ���˵����ȷ����acd��
a����������ͬʱ����п��ȡ���������ʱȴ�п��
b•����ʱ������ͨ�˵�����Ϊ���������Է�ֹ�����ĸ���
c������Ũ������ʯ�Ҷ�H2���и������
d•��ʼʵ��ʱ��Ӧ��ͨ��H2����������Ƽ���
��ֹͣʵ��ʱ��Ӧ��ֹͣͨ��H2����ֹͣ����•
��������衿
��2������ʵ���в��������������ƻ��⻯�ƶ����ܱ���������С���ͬѧ�Է�Ӧ��Ĺ������ɷ�������¼��裮
����l������Ca ��CaH2��
����2������CaH2��CaO��
����3������Ca��CaH2��CaO��
�����ʵ�鷽������֤���衿
��3������ʵ���û�ѧ��������Ca��CaH2�������ʵ������±������ݣ�
| ʵ�鲽�裨��Ҫ��д����������̣� | Ԥ������ͽ��� |
| ȡ����������Ʒ��•�� |
��ȡm1g��Ʒ��ˮ��ȫ��Ӧ��������ͼװ�òⶨ���ɵ��������ʱ����aʱ�����ռ�������ĸ��
a�տ�ʼ������ʱ
b������������ʱ
c���徭���鴿�����ռ�
�����װ�����������ã�������ȷ����ͬѧ��Ϊ������Һ����룬�������������ⶨƫ���������⻯�Ƶ���������ƫ�ߣ��조ƫ�ߡ�����ƫ�͡�����Ӱ�족��
����˼�뽻����
��5����ɽ�˶�Ա�����⻯����Ϊ��Դ�ṩ������������ȣ����ŵ����⻯���ǹ��壬Я�����㣮��Ȼ��������ˮ��ӦҲ������������Ϊʲô��Ҫ���������Ʊ����⻯���أ���Ĺ۵��ǵ������ĸ����⻯���У��⻯�Ʋ����������࣮
���� ��1��a������������ͬʱ����п����Һ�л��γ�ԭ��أ���Ӧ���ʼӿ죻
b���������ڼ��ȵ��������뵪����Ӧ��
c��Ũ������ʯ����H2����Ӧ��������ˮ�����Կ��Զ��������и��
d����ͨ��H2�������ų���������ֹ�Ʊ�����������
��2�������ƻ��⻯�ƶ����ܱ���������Ӧ��Ĺ������ɷֿ���ΪCa��CaH2��CaO���е����֣�Ҳ����Ϊ���֣�
��3���⻯���ڸ�����������������Ӧ��ˮ���ɣ�ͨ��װ����ˮ����ͭ�ĸ�����У�����ͭ����������������֣�
��4���ٲⶨ���ɵ��������ʱ����Ӹտ�ʼ���ռ���������Ӧ����ƿ�ڻ������������ԭ�����еĿ�������������Ż������䣻
����Һ��������������ų���������������ⶨ��ݴ��жϣ�
��5�����ݸ���ˮ��Ӧ�ķ���ʽ���⻯����ˮ��Ӧ�ķ���ʽ�жϵ������ĸ����⻯�Ʋ����������Ķ��٣�
��� �⣺��1��a������������ͬʱ����п����Һ�л��γ�ԭ��أ���Ӧ���ʼӿ죬��a��ȷ��
b���������ڼ��ȵ��������뵪����Ӧ����b����
c��Ũ������ʯ����H2����Ӧ��������ˮ�����Կ��Զ��������и����c��ȷ��
d����ͨ��H2�������ų���������ֹ�Ʊ�������������d��ȷ��
��ѡacd��
��2�������ƻ��⻯�ƶ����ܱ���������Ӧ��Ĺ������ɷֿ���ΪCa��CaH2��CaO���е����֣�Ҳ����Ϊ���֣����Լ���3ΪCa��CaH2��CaO��
�ʴ�Ϊ��Ca��CaH2��CaO��
��3���⻯���ڸ�����������������Ӧ��ˮ���ɣ�ͨ��װ����ˮ����ͭ�ĸ�����У�����ͭ����������������֣����Զ��Լ���Ca��CaH2��ʵ�鷽��Ϊȡ��������������������������Ӧ����������ͨ��װ����ˮ����ͭ�ĸ�����У��۲���ˮ����ͭ�Ƿ����ɫ��
�ʴ�Ϊ��ȡ��������������������������Ӧ����������ͨ��װ����ˮ����ͭ�ĸ�����У��۲���ˮ����ͭ�Ƿ����ɫ��
��4���ٲⶨ���ɵ��������ʱ����Ӹտ�ʼ���ռ���������Ӧ����ƿ�ڻ������������ԭ�����еĿ�������������Ż������䣬
��ѡa��
����Һ��������������ų���������������ⶨ������Լ�����⻯�Ƶ���������ƫ�ߣ�
�ʴ�Ϊ��ƫ�ߣ�
��5�����ݸ���ˮ��Ӧ�ķ���ʽΪCa+2H2O=Ca��OH��2+H2�����⻯����ˮ��Ӧ�ķ���ʽΪCaH2+2H2O=Ca��OH��2+2H2�������Ե������ĸ����⻯���У��⻯�Ʋ����������࣬
�ʴ�Ϊ���������ĸ����⻯���У��⻯�Ʋ����������࣮
���� ������Ҫ�������ʵ��Ʊ�����ȷ����������Ϣ����������Ԫ�ػ�����Ļ���֪ʶ�ǽ���Ĺؼ�����Ŀ�Ѷ��еȣ�

 53���ò�ϵ�д�
53���ò�ϵ�д�| A | ʵ������������Ϊ�˼ӿ췴Ӧ���ʣ�����ϡH2SO4�еμ�����Cu��NO3��2��Һ | |
| B | Ϊ������¯ˮ���е�CaSO4�������ñ���Na2CO3��Һ���ݣ��ټ��������ܽ� | |
| C | N2��g��+3H2��g��?2NH3��g����H��0��������������ʱ�����¶ȣ�ƽ��ʱ����ת�������� | |
| D | ���ȷ�Ӧ��TiO2��s��+2Cl 2��g��=TiCl4��g��+O2��g������һ�������¿��Է����У� ��÷�Ӧ�ġ�S��0 |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� |  | B�� |  | C�� |  | D�� | ����� |
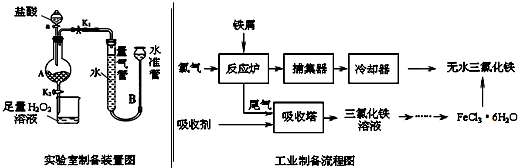
��֪����1����ˮFeCl3���۵�Ϊ555K���е�Ϊ588K��
��2������м�е����ʲ������ᷴӦ
��3����ͬ�¶�����ˮ���Ȼ�����ˮ�е��ܽ�����£�
| �¶�/�� | 0 | 20 | 80 | 100 |
| �ܽ�ȣ�g/100g H2O�� | 74.4 | 91.8 | 525.8 | 535.7 |
���ɼ�K1���رյ��ɼ�K2��������a�������μ����ᣮ
����ʱ���رյ��ɼ�K1�����ɼ�K2����A����Һ��ȫ�����ձ���رջ���a��
���ձ�����Һ����һϵ�в�����õ�FeCl3•6H2O���壮��ش�
��1��ʵ�����Ʊ�װ��ͼ�У���A�м�������������Ƿ�Һ©�����ձ��м���������H2O2��Һ�������ǣ������ӷ���ʽ��ʾ��2Fe2++H2O2+2H+=2Fe3++2H2O��
��2��Ϊ�˲ⶨ����м������������������ʹ����ȫ�����ᷴӦ�������ұ�װ�òⶨ���ɵ��������������������С�������������װ��A�в��������ݻ������ܺ�ˮ��Һ�治�䣮
��3����ҵ�Ʊ��з�Ӧ¯�з�����Ӧ�Ļ�ѧ����ʽΪ2Fe+3Cl2=2FeCl3������������FeCL2��Һ�����ռ�����β������Ӧ�����ӷ���ʽ2Fe2++Cl2=2Fe3+��
��4����ҵ�Ʊ������У������Ȼ�����Һ���FeCL3.6H2O�IJ����Ǽ���ϡ���������Ũ������ȴ�ᾧ�����ˣ�
��5��FeCl3����������ͨ�����õ������ⶨ����ȡm g��ˮ�Ȼ�����Ʒ������ϡ���ᣬ���Ƴ�100mL��Һ��ȡ��10.00mL�������Թ�����KI��Һ����ַ�Ӧ���뼸�ε�����Һ������c mol•L-1 Na2S2O3��Һ�ζ�������V mL��[��֪��I2+2S2O32-�T2I-+S4O62-��M��FeCL3��=162.5g/mol��]
��������Һʱ��Ҫ����������ƽ�������룩��ҩ�ס��ձ�������������ͷ�ιܡ�100mL������ƿ��
����Ʒ���Ȼ�������������$\frac{162.5cV}{m}$%��


 ��
��