题目内容
【化学与技术】
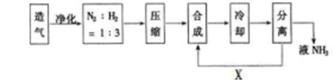
下图表示某些化工生产的流程(有的反应条件和产物已略去)

请回答下列问题:
(1)流程中所涉及的化学工业 (写出两个即可)。
(2)反应I需在500℃进行,主要原因是 ;实际工业生产中,反应Ⅱ的条件是 。
(3)写出反应III的化学方程式 。
(4)工业上,析出K后,再向母液中继续通入E,并加入细小食盐颗料,其目的是 。
(5)工业上常用Na2CO3溶液吸收制取HNO3产生的尾气中的NO2,生成NaNO3、NaNO2和一种气体,写出反应的化学方程式 。
下图表示某些化工生产的流程(有的反应条件和产物已略去)

请回答下列问题:
(1)流程中所涉及的化学工业 (写出两个即可)。
(2)反应I需在500℃进行,主要原因是 ;实际工业生产中,反应Ⅱ的条件是 。
(3)写出反应III的化学方程式 。
(4)工业上,析出K后,再向母液中继续通入E,并加入细小食盐颗料,其目的是 。
(5)工业上常用Na2CO3溶液吸收制取HNO3产生的尾气中的NO2,生成NaNO3、NaNO2和一种气体,写出反应的化学方程式 。
(1)合成氨,氨氧化法制硝酸,联合制碱法(或侯氏制减法)
(2)500℃时,该反应的催化剂的活性最高;铂铑合金作催化剂,高温
(3)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
(4)增大NH4+和Cl-的浓度,析出副产品NH4Cl
(5)2NO2+Na2CO3=NaNO3+NaNO2+CO2
(2)500℃时,该反应的催化剂的活性最高;铂铑合金作催化剂,高温
(3)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
(4)增大NH4+和Cl-的浓度,析出副产品NH4Cl
(5)2NO2+Na2CO3=NaNO3+NaNO2+CO2
依据流程分析液态空气蒸馏得到氧气和氮气,焦炭和水蒸气反应生成氢气和一氧化碳;推断反应Ⅰ是合成氨的反应,所以A为O2、B为N2、C为H2、E为NH3,反应Ⅱ是氨气的催化氧化反应生成G为NO,H为NO2、I为HNO3,L为NH4NO3,D为CO,F为CO2;E+F+饱和食盐水=NaHCO3↓+NH4Cl,Ⅲ反应是工业侯德榜制碱法;K为NaHCO3,M为Na2CO3;J为NH4Cl;
(1)流程分析推断反应Ⅰ是工业合成氨;Ⅱ是工业上制硝酸的第一步氨气的催化氧化;Ⅲ是工业上候氏制碱法或联合制碱法;
(2)反应I合成氨是放热反应,需在500℃进行是为了提高反应速率,催化剂活性最大;实际工业生产中,反应Ⅱ的条件是铂铑合金做催化剂高温加热进行氨气的催化氧化反应;
(3)反应Ⅲ是候氏制碱法的反应原理,氨化的饱和食盐水中通入二氧化碳生成碳酸氢钠晶体和氯化铵,反应的化学方程式为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl;
(4)工业上,析出NaHCO3后,再向母液中继续通入NH3,并加入细小食盐颗料,是为了增大铵根离子和氯离子浓度,降低氯化铵的溶解度利于晶体析出;
(5)根据信息产物知,反应方程式是2NO2+Na2CO3=NaNO3+NaNO2+CO2。
(1)流程分析推断反应Ⅰ是工业合成氨;Ⅱ是工业上制硝酸的第一步氨气的催化氧化;Ⅲ是工业上候氏制碱法或联合制碱法;
(2)反应I合成氨是放热反应,需在500℃进行是为了提高反应速率,催化剂活性最大;实际工业生产中,反应Ⅱ的条件是铂铑合金做催化剂高温加热进行氨气的催化氧化反应;
(3)反应Ⅲ是候氏制碱法的反应原理,氨化的饱和食盐水中通入二氧化碳生成碳酸氢钠晶体和氯化铵,反应的化学方程式为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl;
(4)工业上,析出NaHCO3后,再向母液中继续通入NH3,并加入细小食盐颗料,是为了增大铵根离子和氯离子浓度,降低氯化铵的溶解度利于晶体析出;
(5)根据信息产物知,反应方程式是2NO2+Na2CO3=NaNO3+NaNO2+CO2。

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案
相关题目


 式______________。
式______________。