题目内容
25℃时,下列溶液中微粒的物质的量浓度关系正确的是
A. 0.1mol·L-1NaHC2O4溶液(pH=5.5):c(Na+)> c(HC2O4-)> c(H2C2O4)> c(C2O42-)
B. 0.1mol·L-1NaHS溶液:c(OH-)+ c(S2-)= c(H+)+ c(H2S)
C. 0.1mol·L-1CH3COOH溶液和0.1mol·L-1CH3COONa溶液等体积混合:c(Na+)> c(CH3COOH)> c(CH3COO-)> c(H+)> c(OH-)
D. 0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1NaOH溶液至中性:c(Na+)> c(SO42-)>c(NH4+)> c(OH-)= c(H+)
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案钠及其化合物具有广泛的用途。
(1)工业上制备金属钠的常用方法是_______。试写出制备金属钠的化学方程式_____________。金属钠可用于________________(写出Na在熔点低方面的一种用途)。
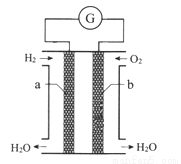
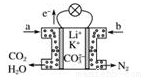
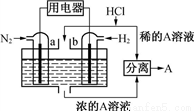
(2)用Na2CO3熔融盐作电解质,CO、O2、CO2为原料可组成新型电池。该电池的结构如图所示:

①正极的电极反应式为_______,电池工作时物质A可循环使用,A物质的化学式为_______。
②请写出检验Na2CO3中钠元素的方法_________________________。
(3)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 11.6 | 10.3 | 11.1 |
上述盐溶液的阴离子中,结合H+能力最强的是_________,根据表中数据,浓度均为0.01 mol·L-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是_______(填序号)。
a.HCN b.HClO c.CH3COOH d.H2CO3
(4)实验室中常用NaOH来进行尾气处理、洗气和提纯。
①常温下,当300 mL 1 mol·L-1的NaOH溶液吸收4.48 L(折算成标准状况)SO2时,所得溶液pH>7,则溶液中各离子浓度由大到小的顺序为_______。
②已知几种离子开始沉淀时的pH如下表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加某浓度的NaOH溶液时,_______(填离子符号)先沉淀,Ksp_______Ksp(填“>”、“=”或“<”)。
甲酸钙广泛用于食品、化工、石油等工业生产上,300~400℃左右分解。
Ⅰ、实验室制取的方法之一是:Ca(OH)2 +2HCHO + H2O2 = Ca(HCOO)2 + 2H2O + H2↑。实验室制取时,将工业用氢氧化钙和甲醛依次加入到质量分数为30-70%的过氧化氢溶液中(投料物质的量之比依次为1∶2∶1.2),最终可得到质量分数98%以上且重金属含量极低的优质产品。
(1)过氧化氢比理论用量稍多,其目的是__________。
(2)反应温度最好控制在30-70℃之间,温度不易过高,其主要原因是__________。
(3)制备时在混合溶液中要加入微量硼酸钠抑制甲醛发生副反应外,还要加入少量的Na2S溶液,加硫化钠的目的是__________。
(4)实验时需强力搅拌45min,其目的是__________;结束后需调节溶液的pH 7~8,其目的是__________。最后经结晶分离、干燥得产品。
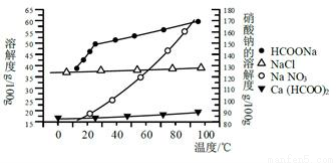
Ⅱ、某研究性学习小组用工业碳酸钙(主要成分为CaCO3;杂质为:Al2O3、FeCO3) 为原料,先制备无机钙盐,再与甲酸钠溶液混合制取甲酸钙。结合如图几种物质的溶解度曲线及表中相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算),现提供的试剂有:A.甲酸钠,B.5mol·L-1硝酸,c.5mol·L-1盐酸,d.5mol·L-1硫酸,e.3%H2O2溶液,f.澄清石灰水。
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
请补充完整由碳酸钙制备甲酸钙的实验步骤 :
步骤1.称取13.6g甲酸钠溶于约20mL水,配成溶待用,并称取研细的碳酸钙样品10g待用。
步骤2._________。
步骤3._________。
步骤4.过滤后,将滤液与甲酸钠溶液混合,调整溶液pH 7~8,充分搅拌,所得溶液经蒸发浓缩、__________、洗涤、60℃时干燥得甲酸钙晶体。
X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如下图所示:
X | Y | |
Z | W |
请回答下列问题:
(1)W位于周期表中第__________周期,第____族;
(2)X可形成双原子分子,其分子的电子式是_____;Y和氢元素形成的10电子微粒中常见+1价阳离子为_____(填化学式,下同);Z和氢元素形成的18电子微粒中常见的-1价阴离子为______;
(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式______________________。
(4)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡时有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式是_____________。




 C B. 溴化铵的电子式:
C B. 溴化铵的电子式:
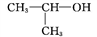
 D. 2-丙醇的结构简式:
D. 2-丙醇的结构简式: