题目内容
【题目】铁黑(Fe3O4)是常见的铁系颜料.一种制取铁黑的实验流程如下图所示:
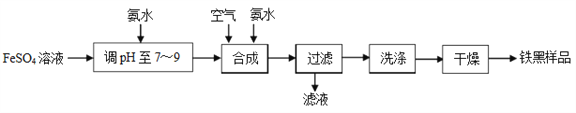
制取铁黑的反应原理可表示为Fe(OH)2+2Fe(OH)3![]() Fe(OH)2·2Fe(OH)3
Fe(OH)2·2Fe(OH)3![]() Fe3O4
Fe3O4
(1)加入氨水调pH至7~9时,发生反应的离子方程式为_______________。
(2)为了保证铁黑样品的质量,“合成”中需要控制的因素有______________(填三个)。
(3)铁黑产品中Fe3O4的含量是判断产品等级的依据之一。某铁黑样品中混有的杂质为FeO、Fe2O3中的一种。根据国标方法,进行的测定实验如下:
步骤1:称取1.908g样品置于锥形瓶中,加入足量盐酸,加热使之完全溶解。
步骤2:向锥形瓶中先加入足量的SnCl2溶液,将Fe3+全部转化为Fe2+,除去过量的Sn2+,再加入一定量的硫酸和磷酸,并滴加指示剂。
步骤3:再向锥形瓶中滴加0.08200mol·L-1K2Cr2O7溶液,发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
恰好完全反应时,共消耗50.00mL K2Cr2O7溶液。请计算样品中Fe3O4的质量分数_____________(写出计算过程)。
【答案】 Fe2+ + 2NH3·H2O = Fe(OH)2↓+ 2NH4+ 氨水的用量、通入空气的量(或氢氧化亚铁与空气的比例)、反应温度等 n(Fe2+)=6n(Cr2O72-)=6×0.08200mol·L-1×50.00×10-3 L=0.0246mol
1.908g样品中铁元素总质量为:m(Fe)= 0.0246mol×56 g·mol -1=1.3376g
1.908g样品中氧元素总质量为:m(O)= 1.908g -1.3376g=0.5304g
n(O)= 0.5304g/16 g·mol -1=0.03315mol
n(O)/n(Fe)=1.348>4/3,所以铁黑样品中混有的杂质为Fe2O3
设Fe3O4的物质的量为x,Fe2O3的物质的量为y
![]()
x=0.0076mol,y=0.0009mol
样品中Fe3O4的质量分数=![]() =92.41%
=92.41%
【解析】(1)在FeSO4溶液中滴加氨水调pH至7~9时,会有生成Fe(OH)2,发生反应的离子方程式为Fe2+ + 2NH3·H2O = Fe(OH)2↓+ 2NH4+;
(2)Fe(OH)2在空气中易氧化而生成Fe(OH)3,为保证铁黑样品的质量,“合成”中需要控制的因素有氨水的用量、通入空气的量(或氢氧化亚铁与空气的比例)、反应温度等。
(3)n(Fe2+)=6n(Cr2O72-)=6×0.08200mol·L-1×50.00×10-3 L=0.0246mol
1.908g样品中铁元素总质量为:m(Fe)= 0.0246mol×56 g·mol -1=1.3376g
1.908g样品中氧元素总质量为:m(O)= 1.908g -1.3376g=0.5304g,n(O)= 0.5304g/16 g·mol -1=0.03315mol;
n(O)/n(Fe)=1.348>4/3,所以铁黑样品中混有的杂质为Fe2O3
设Fe3O4的物质的量为x,Fe2O3的物质的量为y;
3x+2y=0.0246mol、4x+3y=0.03315mol 解得:x=0.0076mol、y=0.0009mol;
则样品中Fe3O4的质量分数=![]() ×100%=92.41%。
×100%=92.41%。

【题目】将绿豆大小方形金属钠,投入足量且含酚酞的水中,根据相应现象不能得出的结论是 ( )
选项 | 实验现象 | 结论 |
A | 方形金属钠变成小球 | 方形钠反应速率快 |
B | 钠浮于水面游动 | 水的密度大于钠 |
C | 酚酞溶液变成红色 | 有NaOH生成 |
D | 钠球游动,有吱吱声 | 有气体生成 |