题目内容
【题目】反应A(?)+aB(g)C(g)+2D(g)(a为正整数).反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图所示.下列说法不正确的是( ) 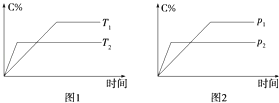
A.若a=2,则A为液态或固体
B.该反应的正反应为放热反应
C.T2>T1 , P2>P1
D.其他条件不变,增加B的物质的量,平衡正向移动,平衡常数K增大
【答案】D
【解析】解:A.根据图2,压强变大,C的百分含量减小,平衡向左移动,所以反应前气态物质的化学计量数之和小于反应后气态物质的化学计量数之和,即若a=2,则A为液态或固体,故A正确;
B.根据图1,温度升高,C的百分含量减小,平衡向左移动,所以该反应为放热反应,故B正确;
C.根据图1,T2时反应时间短,速率快,所以T2>T1;根据图2,P2时反应时间短,速率快,所以 P2>P1 , 故C正确;
D.K与反应物的量无关,只受温度的影响,所以其他条件不变,增加B的物质的量,平衡常数K不变,故D错误;
故选D.

 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程: 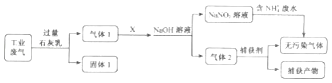
(1)固体I中主要成分为 , 捕获剂所捕获的气体主要是 .
(2)处理含NH4+废水时,发生反应的离子方程式为 .
(3)若X为适量空气,严格控制空气用量的原因是 .
(4)工业废气中的SO2、NO还可采用NaClO2溶液作为吸收剂进行净化,在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10﹣3molL﹣1 . 反应一段时间后溶液中离子浓度的分析结果如表:
离子 | SO42﹣ | SO32﹣ | NO3﹣ | NO2﹣ | Cl﹣ |
c(molL﹣1) | 8.35×10﹣4 | 6.87×10﹣6 | 1.5×10﹣4 | 1.2×10﹣5 | 3.4×10﹣3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式 .
增加压强,NO的转化率(填“提高”、“不变”或“降低”).
②随着吸收反应的进行,吸收剂溶液的pH逐渐(填“增大”、“不变”或“减小”).
③如果采用NaClO、Ca(ClO)2替代NaClO2 , 也能得到较好的烟气脱硫效果.从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是 .