题目内容
【题目】完成下列各问题
(1)泡沫灭火器中的药品为NaHCO3和Al2(SO4)3,其反应的离子方程式为:________;
(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出①电荷守恒__________________;②物料守恒______________________;③质子守恒______________________________;④下列粒子浓度由大到小的顺序为c(Na+)、c(HCO3-)、c(CO32-),c(H2CO3)、c(OH-)______。
【答案】 3HCO3-+Al3+=Al(OH)3↓+3CO2↑ c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) c(H+)+c(H2CO3)=c(OH-)+c(CO32-) c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-)
【解析】试题分析:本题考查双水解离子方程式的书写,盐溶液中电荷守恒、物料守恒、质子守恒的书写,盐溶液中粒子浓度大小的比较。
(1)Al2(SO4)3属于强酸弱碱盐,由于Al3+的水解Al2(SO4)3溶液呈酸性;NaHCO3溶液中由于HCO3-的水解程度大于电离程度,溶液呈碱性;Al2(SO4)3溶液与NaHCO3溶液混合,由于Al3+、HCO3-水解互相促进,最终Al3+、HCO3-的水解趋于完全生成白色Al(OH)3沉淀和CO2气体,反应的离子方程式为3HCO3-+Al3+=3CO2↑+Al(OH)3↓。
(2)NaHCO3在水溶液中的电离方程式为NaHCO3=Na++HCO3-、HCO3-![]() H++CO32-,在NaHCO3溶液中还存在HCO3-的水解平衡:HCO3-+H2O
H++CO32-,在NaHCO3溶液中还存在HCO3-的水解平衡:HCO3-+H2O![]() H2CO3+OH-和水的电离平衡:H2O
H2CO3+OH-和水的电离平衡:H2O![]() H++OH-。①电荷守恒指溶液中阴离子所带负电荷总数一定等于阳离子所带正电荷总数,电荷守恒为c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)。②物料守恒根据Na、C守恒书写,物料守恒为c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)。③质子守恒指:电解质溶液中,电离、水解等过程中得到的质子(H+)数等于失去的质子(H+)数,对NaHCO3溶液可分析为:
H++OH-。①电荷守恒指溶液中阴离子所带负电荷总数一定等于阳离子所带正电荷总数,电荷守恒为c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)。②物料守恒根据Na、C守恒书写,物料守恒为c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)。③质子守恒指:电解质溶液中,电离、水解等过程中得到的质子(H+)数等于失去的质子(H+)数,对NaHCO3溶液可分析为: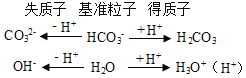 ,质子守恒为c(H+)+c(H2CO3)=c(OH-)+c(CO32-)。④HCO3-的水解程度和电离程度都很微弱,且HCO3-的水解程度大于电离程度,溶液中粒子浓度由大到小的顺序为:c(Na+)> c(HCO3-)> c(OH-)> c(H2CO3)> c(CO32-)。
,质子守恒为c(H+)+c(H2CO3)=c(OH-)+c(CO32-)。④HCO3-的水解程度和电离程度都很微弱,且HCO3-的水解程度大于电离程度,溶液中粒子浓度由大到小的顺序为:c(Na+)> c(HCO3-)> c(OH-)> c(H2CO3)> c(CO32-)。

【题目】某研究性学习小组同学为了探究“在相同的温度和压强下、相同体积的任何气体都含有相同数目和分子”,他们设计了如下实验装置并记录相关实验数据。实验装置:
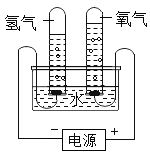
部分实验数据:
温度 | 压强 | 时间 | 水槽中H2O的质量 | H2体积 | O2体积 |
30℃ | 101 kPa | 0 | 300 g | 0 | 0 |
30℃ | 101 kPa | 4分钟 | 298.2 g | 1.243 L |
请回答下列问题:
(1)4分钟时H2、O2物质的量分别是__________mol、___________mol。
(2)该温度下,气体摩尔体积是________________。
(3)假设电解H2O速率相同,2分钟时试管内收集到的H2的体积是___________mL。
(4)根据以上实验得出如下结论,其中不正确的是_________________。
A. 气体摩尔体积与气体的温度相关
B. 在该实验条件下,3 mol O2的气体摩尔体积为74.58 L/mol
C. 同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D. 该实验条件下,O2的密度为1.287 g/L