题目内容
【题目】铜基及硼系高温超导材料都具有良好的应用前景。回答下列问题:
(1)写出Cu原子价电子的轨道表达式:____________。BF3的立体构型是____________。
(2)NaBH4被认为是有机化学上的“万能还原剂”, NaBH4电子式为____________,其中三种元素的第一电离能由大到小的顺序是_________________。
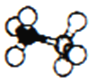
(3)BH3·NH3是一种有效、安全的固体储氢材料,结构如右图所示。 B原子的轨道杂化类型是____________。该物质中含有配位键,其中提供空轨道接受孤对电子的是____________。该物质易溶于水,其原因是____________。
(4)硼与氦形成类似苯的化合物B3N3H6(硼氮苯),俗称无机苯。硼氮苯属于分子____________(填“极性”或“非极性”),一个硼氮苯分子中有____________个σ键,形成π键的电子由____________提供。
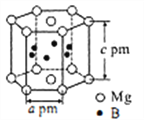
(5)硼与镁形成的高温超导材料晶体结构如图所示。该六方晶胞中镁原子与硼原子的数量比为____________,晶体密度d=____________g·cm-3。
【答案】 ![]() 平面三角形
平面三角形 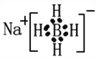 H>B>Na sp3杂化 B原子 该分子属于极性分子,且与水分子之间能形成氢键 非极性 12 N原子 1∶2
H>B>Na sp3杂化 B原子 该分子属于极性分子,且与水分子之间能形成氢键 非极性 12 N原子 1∶2 ![]() 或
或 ![]() ×107
×107
(计算式为 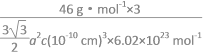 )
)
【解析】(1)铜的原子序数是29,根据核外电子排布规律可知Cu原子价电子的轨道表达式为![]() 。BF3中B中性原子的价层电子对数是3,且不存在孤对电子,所以立体构型是平面三角形。(2)NaBH4是离子化合物, NaBH4电子式为
。BF3中B中性原子的价层电子对数是3,且不存在孤对电子,所以立体构型是平面三角形。(2)NaBH4是离子化合物, NaBH4电子式为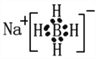 ,非金属性越强,第一电离能越大,则其中三种元素的第一电离能由大到小的顺序是H>B>Na。(3)BH3·NH3是一种有效、安全的固体储氢材料,结构如右图所示。
,非金属性越强,第一电离能越大,则其中三种元素的第一电离能由大到小的顺序是H>B>Na。(3)BH3·NH3是一种有效、安全的固体储氢材料,结构如右图所示。
B形成的3个共价键,一个配位键,所以B原子的轨道杂化类型是sp3杂化。该物质中含有配位键,其中提供空轨道接受孤对电子的是B。该分子属于极性分子,且与水分子之间能形成氢键,因此该物质易溶于水。(4)苯是非极性分子,所以硼氮苯属于非极性分子。单键都是σ键,双键中含有一个σ键,则一个硼氮苯分子中有12个σ键。B原子最外层电子数是3个,因此形成π键的电子由氮原子提供。(5)根据晶胞结构可知Mg原子个数=2×1/2+12×1/6=3,B全部在晶胞中,则该六方晶胞中镁原子与硼原子的数量比为1∶2,晶体的体积是![]() ,所以晶体密度d=
,所以晶体密度d=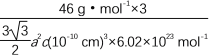 g·cm-3。
g·cm-3。

 阅读快车系列答案
阅读快车系列答案