题目内容
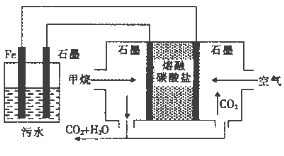
【题目】电浮选凝聚法处理酸性污水的工作原理如图。下列说法正确的是
A. 左侧装置中的铁电极可换成石墨电极
B. 通入甲烷的石墨电极的电极反应式为: CH4+4CO32——8e—=5CO2+2H2O
C. 通入空气的石墨电极做正极,发生氧化反应
D. 若左侧装置中石墨电极产生标况下气体44.8L气体, 则消耗2mol甲烷
【答案】B
【解析】在甲烷燃料电池中,通入甲烷的一极为原电池的负极,发生氧化反应,电极方程式为CH4+ 4CO32--8e-=5CO2+2H2O,通入空气(氧气)的一极为原电池的正极,发生还原反应,电极方程式为O2+ 2CO2+4e-=2CO32-,铁连接原电池的正极,为电解池的阳极,被氧化,发生Fe-2e-=Fe2+,阴极生成2H++ 2e-=H2↑,A.铁连接原电池的正极,为电解池的阳极,被氧化,电极反应为Fe-2e-=Fe2+,因此左侧装置中的铁电极不能换成石墨电极,A错误; B.甲烷的一极为原电池的负极,发生氧化反应,电极方程式为CH4+4CO32--8e-=5CO2+2H2O,B正确;C. 通入空气的石墨电极做正极,发生还原反应,C错误;D. 左侧装置中石墨电极是阴极,氢离子放电,产生标况下气体44.8L气体, 即H2是2mol,转移4mol电子,根据电子转移守恒可知消耗甲烷4mol÷8=0.5mol,D错误;答案选B。

【题目】实验室里保存下列试剂,其保存的方法和理由,描述都正确的是
编号 | 试剂 | 保存方法 | 理由 |
A | 水玻璃 | 存放在带橡皮塞的细口瓶中,密封 | 防止与空气接触被氧化和与二氧化碳接触而变质 |
B | 硫酸亚铁晶体 | 存放在带玻璃塞的广口瓶中,密封 | 防止与空气接触被氧化 |
C | 浓硫酸 | 密闭保存 | 防止吸水和挥发 |
D | 新制的溴水 | 存放在无色试剂瓶中,密封 | 防止挥发 |
A. A B. B C. C D. D