题目内容
【题目】如果Fe3+、SO42-、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是 ( )
A. Na+ B. PO43- C. CO32- D. Cl-
【答案】D
【解析】Fe3+、SO42-、Al3+和M四种离子以物质的量之比为2:4:1:1共同存在于同一种溶液中,由电荷守恒可知,3×2+3×1>2×4,则M为阴离子,设电荷数为x,则3×2+3×1=2×4+x×1,解得x=1,又因为铁离子、铝离子与碳酸根、磷酸根离子均反应,不能共存,所以M是氯离子,答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】按要求回答问题
(1)KAl(SO4)2的电离方程式_______________________。
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是______________、_________________ (填微粒符号)。
(3)实验室用质量分数为36.5%,密度为1.19g·cm-3的浓盐酸来配制100ml,2mol/L的稀盐酸,需要用量筒量取_______________ml该浓盐酸。
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L(标况) SO2时,转移的电子是__________mol。
(5)下列四个图像中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。
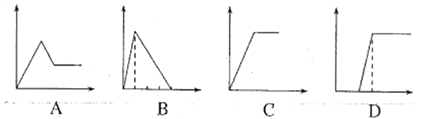
溶液 | 加入的物质 | 序号 |
①AlCl3溶液 | 通入过量的NH3 | ___ |
②Na2CO3和NaOH的溶液 | 滴入过量的盐酸 | ___ |
③NaAlO2溶液 | 滴加稀硫酸至过量 | ___ |