��Ŀ����
����Ŀ����ѧ��Ӧ�Ŀ������ȶ�����������������Ҫ�����塣
��1����Ӱ�췴Ӧ�����������ڿո�
ʵ �� | Ӱ������ |
�� ʳ����ڱ��������ӳ������� | ��__________ |
�� ʵ���ҽ���״ҩƷ��ϸ���ٽ��з�Ӧ | ��__________ |
�� ��H2O2�ֽ���O2ʱ������MnO2 | ��__________ |
�� ʵ�����Ʊ�H2ʱ���ý�Ũ��������Zn����Ӧ | ��__________ |
��2����ͼ��ʾ��800��ʱA��B��C�����������ܱ������з�Ӧʱ��Ũ�ȱ仯������ͼ�ش����⣺
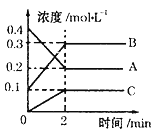
�ٸ÷�Ӧ��������_______________��
��2min�ڣ�C�ķ�Ӧ����Ϊ____________________��
�۸÷�Ӧ�ķ���ʽΪ__________________________��
�������������£����A�ķ�Ӧ����Ϊ0.05mol/(L��s)����ʱ�ķ�Ӧ��800��ʱ��ȣ�______________��
A����800��ʱ�� B����800��ʱ�� C����800��ʱ����һ��
���𰸡��¶� �������� ���� Ũ�� B�� C 0.05 mol /��L��min�� 2A![]() 2B+C B
2B+C B
��������
��1��Ӱ�컯ѧ��Ӧ���ʵ��������¶ȡ�Ũ�ȡ������Լ�����ı������С�ȣ���ʵ���Ŀ�Ŀ���ѡ��Ĵ�ʩ��
��2����ͼ���֪��A�����ʵ���Ũ�ȼ�С��B��C�����ʵ���Ũ�����ӣ���AΪ��Ӧ�B��CΪ������ɷ�Ӧ��Ũ�ȵı仯֮�ȵ��ڻ�ѧ������֮�ȿɵã���c��A������c��B������c��C��=0.2mol/L��0.2mol/L��0.1mol/L=2��2��1����Ӧ�Ļ�ѧ����ʽΪ2A![]() 2B+C��������=
2B+C��������=![]() ���㷴Ӧ���ʣ�
���㷴Ӧ���ʣ�
��1���ٱ������¶Ƚϵͣ������¶ȣ���Ӧ���ʼ�С�����ӳ������ڣ�
�𰸣��¶ȣ�
�ڹ��������Ĵ�СӰ�컯ѧ��Ӧ���ʣ������Խ��Ӧ����Խ�죬ʵ���ҽ���״ҩƷ��ϸ���ɼӿ췴Ӧ���ʣ�
�𰸣�����������
�۴����ܼӿ췴Ӧ���ʣ���H2O2�ֽ���O2ʱ������MnO2�����������ã��ܽϿ��������壻
�𰸣�������
�ܶ�����Һ�еĻ�ѧ��Ӧ������Ӧ��Ũ���ܼӿ췴Ӧ���ʣ��ý�Ũ��������Zn����Ӧ�������������������ʣ���Ũ�Ȳ��ܹ�������Ũ������������������
�𰸣�Ũ�ȣ�
��2������ͼ���֪��A�����ʵ���Ũ�ȼ�С��B��C�����ʵ���Ũ�����ӣ���AΪ��Ӧ�B��CΪ�����
�𰸣�B��C
����(C)=![]() =
=![]() =0.05mol/��Lmin����
=0.05mol/��Lmin����
�𰸣�0.05mol/��Lmin��
���ɷ�Ӧ��Ũ�ȵı仯֮�ȵ��ڻ�ѧ������֮�ȿɵã���c��A������c��B������c��C��=0.2mol/L��0.2mol/L��0.1mol/L=2��2��1����Ӧ�Ļ�ѧ����ʽΪ2A![]() 2B+C��
2B+C��
�𰸣�2A2B+C��
�ܵ�A�ķ�Ӧ����Ϊ0.05mol/��Ls��������C��ʾ������Ϊ������C��=0.025mol/��Ls��=1.5 mol/��Lmin�������ݢڵĽ���ԣ�C��=0.05mol/��Lmin������ʱ�ķ�Ӧ��800��ʱ��ȣ���800��ʱ�죻
�𰸣�B