题目内容
9.已知下列反应的反应热:(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ•mol-1
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ•mol-1
则下列反应的反应热为( )
2C(s)+2H2(g)+O2(g)═CH3COOH(l)
| A. | △H=+488.3 kJ•mol-1 | B. | △H=-244.15 kJ•mol-1 | ||
| C. | △H=-977.6 kJ•mol-1 | D. | △H=-488.3 kJ•mol-1 |
分析 根据燃烧热写出热化学方程式,再利用盖斯定律来计算反应2C(s)+2H2(g)+O2(g)=CH3COOH(1)的反应热.
解答 解:由(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ•mol-1
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ•mol-1
由盖斯定律可知,(3)×2+(2)×2-(1)可得反应2C(s)+2H2(g)+O2(g)=CH3COOH(1),
其反应热为2×(-285.8kJ•mol-1)+2×(-393.5kJ•mol-1)+870.3kJ•mol-1=-488.3KJ•mol-1,
故选D.
点评 本题考查学生盖斯定律计算反应热的知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
4.下列关于实验原理或操作的叙述中,正确的是( )
①从碘水中提取单质碘时,可用无水乙醇代替CCl4
②可以用NaOH溶液除去溴苯中的溴杂质
③用酸性KMnO4溶液可以除去乙烯中混有的乙炔
④实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法.
①从碘水中提取单质碘时,可用无水乙醇代替CCl4
②可以用NaOH溶液除去溴苯中的溴杂质
③用酸性KMnO4溶液可以除去乙烯中混有的乙炔
④实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ②④ |
1.两个体积相同的密闭容器一个盛有氯化氢,另一个盛有臭氧,在同温同压下,两个容器内的气体一定相同的( )
| A. | 质量 | B. | 密度 | C. | 分子总数 | D. | 原子总数 |
18.已知298K时,2SO2(g)+O2(g)=2SO3(g)△H=-197kJ/mol,在相同温度下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出的热量Q1;向另一体积相同的密闭容器中通入1molSO2和1molO2,达到平衡时放出的热量Q2;则下列关系正确的是( )
| A. | 2Q2=Q1 | B. | 2Q2<Q1 | C. | Q2<Q1<197kJ | D. | Q2=Q1<197kJ |
19.四个试管中都装有5mL0.1mol•L-1Na2S2O3溶液,分别在不同温度下加入0.1mol•L-1硫酸和一定量水,最先出现浑浊的是( )
| A. | 20℃,5mL硫酸,2mL水 | B. | 20℃,4mL硫酸,3mL水 | ||
| C. | 30℃,4mL硫酸,3mL水 | D. | 30℃,5mL硫酸,2mL水 |
 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.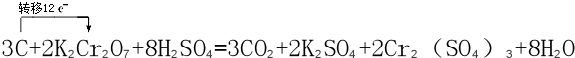
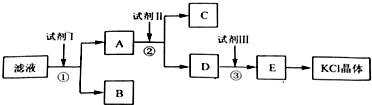
 A、B、C、D、E均为有机物,相互之间存在如图转化关系,且知1mol烯烃 B完全燃烧消耗O2 3mol,E是一种高分子化合物.
A、B、C、D、E均为有机物,相互之间存在如图转化关系,且知1mol烯烃 B完全燃烧消耗O2 3mol,E是一种高分子化合物.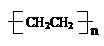 F、CH3COOHG、CH3COOCH2CH3
F、CH3COOHG、CH3COOCH2CH3