题目内容
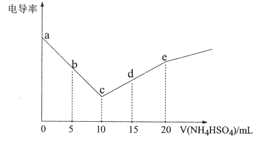
【题目】电导率可用于衡量电解质溶液导电能力的大小。向10mL 0.3 mol·L-1Ba(OH)2溶液滴入0.3 mol·L-1 NH4HSO4溶液,其电导率随滴入的NH4HSO4溶液体积的变化如图所示(忽略BaSO4溶解产生的离子)。下列说法不正确的是
A.a→e的过程水的电离程度逐渐增大
B.b点:c(Ba2+) =0.1 moI.L-1
C.c点:c(NH4+)<c(OH-)
D.d点:c(SO42-)+c(H+)>c(OH-)+c(NH3H2O)
【答案】D
【解析】
ac段电导率一直下降,是因为氢氧化钡和硫酸氢铵反应生成硫酸钡沉淀和一水合氨,c点溶质为一水合氨,ce段电导率增加,是一水合氨和硫酸氢铵反应生成硫酸铵,溶液中的离子浓度增大。
A. a→e的过程为碱溶液中加入盐,水的电离程度逐渐增大,故正确;
B. b点c(Ba2+) = ![]() =0.1 moI.L-1,故正确;
=0.1 moI.L-1,故正确;
C. c点的溶质为一水合氨,一水合氨电离出铵根离子和氢氧根离子,水也能电离出氢氧根离子,所以有c(NH4+)<c(OH-),故正确;
D. d点溶液为等物质的量的一水合氨和硫酸铵,电荷守恒有①c(NH4+)+ c(H+)= 2c(SO42-)+ c(OH-),物料守恒有②c(NH4+)+ c(NH3H2O)=3 c(SO42-),②-①可得c(SO42-)+c(H+)=c(OH-)+c(NH3H2O),故错误。
故选D。

练习册系列答案
相关题目