题目内容
【题目】(1)配制![]() 溶液时为防止其水解,可加入少量________。用离子方程式表示
溶液时为防止其水解,可加入少量________。用离子方程式表示![]() 可作净水剂的原因__________________________________。
可作净水剂的原因__________________________________。
(2)常温下,pH均为11的氢氧化钠溶液和硫化钠溶液中,水电离出的![]() 浓度之比为________。向硫化钠溶液中加入氯化铝时,产生白色沉淀和臭鸡蛋气味的气体,反应的离子方程式为_______________________________________________。
浓度之比为________。向硫化钠溶液中加入氯化铝时,产生白色沉淀和臭鸡蛋气味的气体,反应的离子方程式为_______________________________________________。
(3)在![]() 时,有pH为a的盐酸和pH为b的NaOH溶液,取
时,有pH为a的盐酸和pH为b的NaOH溶液,取![]() 该盐酸,同该NaOH溶液恰好中和,需
该盐酸,同该NaOH溶液恰好中和,需![]() 溶液。若
溶液。若![]() ,则
,则![]() _________。
_________。
(4)用石墨作电极,在![]() 、
、![]() 、
、![]() 、
、![]() 等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
①当阴极放出![]() ,阳极放出
,阳极放出![]() 时,电解质是________。
时,电解质是________。
②当阴极析出金属,阳极放出![]() 时,电解质是________。
时,电解质是________。
③当阴极放出![]() ,阳极放出
,阳极放出![]() 时,电解质是________。
时,电解质是________。
【答案】稀盐酸 ![]()
![]()
![]() 胶体
胶体![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
(1)FeCl3属于强酸弱碱盐,发生FeCl3+3H2O![]() Fe(OH)3+HCl,需要加入少量的稀盐酸,防止水解,净水利用其水解成氢氧化铁胶体,据此分析;
Fe(OH)3+HCl,需要加入少量的稀盐酸,防止水解,净水利用其水解成氢氧化铁胶体,据此分析;
(2)水电离出c(H+)等于水电离出c(OH-),计算碱中水电离出c(OH-),需要计算水电离出的c(H+),Na2S属于弱酸强碱盐,S2-水解,溶液中c(H+)=10-11mol·L-1,根据水的离子积计算水电离出c(OH-),进行分析;
(3)恰好中和,可用n(H+)=n(OH-),据此分析;
(4)根据电解中阴阳离子放电顺序进行分析;
(1) FeCl3属于强酸弱碱盐,发生FeCl3+3H2O![]() Fe(OH)3+HCl,配制
Fe(OH)3+HCl,配制![]() 溶液时为防止其水解,可加入少量稀盐酸;
溶液时为防止其水解,可加入少量稀盐酸;![]() 可作净水剂的原因是发生水解生成氢氧化铁胶体,
可作净水剂的原因是发生水解生成氢氧化铁胶体,![]()
![]()
![]() 胶体
胶体![]() ;
;
答案:稀盐酸;Fe3++3H2O![]() Fe(OH)3(胶体)+3H+;
Fe(OH)3(胶体)+3H+;
(2)NaOH中,水所电离的氢氧根和氢离子数目相同,因为氢氧化钠为强电解质,所以c(H+)=1×10-11mol·L-1;![]() 中,硫化钠为强酸弱碱盐,其中所有氢氧根均由水电离,即
中,硫化钠为强酸弱碱盐,其中所有氢氧根均由水电离,即![]() ,水电离出的c(OH-)浓度之比为
,水电离出的c(OH-)浓度之比为![]() :
:![]() ;向硫化钠溶液中加入氯化铝时,发生双水解,产生白色沉淀氢氧化铝和臭鸡蛋气味的气体硫化氢,方程式为:
;向硫化钠溶液中加入氯化铝时,发生双水解,产生白色沉淀氢氧化铝和臭鸡蛋气味的气体硫化氢,方程式为:![]()
![]() ;
;
答案:10-8;2Al3++3S2-+6H2O=2Al(OH)3↓+3H2↑;
(3)25℃时,有pH为a的HCl溶液和pH为b的NaOH溶液恰好反应,盐酸中n(H+)等于NaOH中n(OH-),则有![]() ,即
,即![]() :
:![]() ,若
,若![]() ,则
,则![]() :
:![]() ;
;
答案:1:10;
(4)①当阴极放出![]() ,阳极放出
,阳极放出![]() 时,实质电解的是水,电解质是
时,实质电解的是水,电解质是![]()
②当阴极析出金属,阳极放出![]() 时,结合放电顺序,电解质是
时,结合放电顺序,电解质是![]() ;
;
③当阴极放出![]() ,阳极放出
,阳极放出![]() 时,电解的是氯化氢,电解质是HCl;
时,电解的是氯化氢,电解质是HCl;
答案为:Na2SO4;CuSO4;HCl。

【题目】某活动小组在实验室探究氨气的的制备方法,并测定其分子组成。
![]() 同学甲用下图所示装置制备氨气。
同学甲用下图所示装置制备氨气。
已知:加热![]() 和
和![]() 饱和溶液可以制取
饱和溶液可以制取![]() 。
。
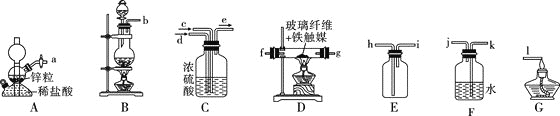
(1)![]() 、D、G处的酒精灯最先点燃的是 ___________
、D、G处的酒精灯最先点燃的是 ___________![]() 填字母
填字母![]() 。
。
(2)写出B中制取![]() 的反应的离子方程式:__________。
的反应的离子方程式:__________。
(3)图示装置从左到右正确连接顺序:![]()
![]() ____
____![]() ____
____![]() ____
____![]() ____
____![]() 。
。
![]() 同学乙用下图所示装置
同学乙用下图所示装置![]() 夹持装置已省略
夹持装置已省略![]() 制备氨气,并与CuO反应测定氨气的组成。
制备氨气,并与CuO反应测定氨气的组成。
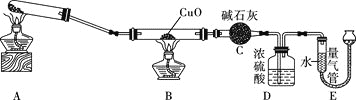
(1)同学乙在相同条件下,选择不同固体试剂制取氨气,实验数据如下:
实验方案 | 固体试剂 |
| |
1 |
|
| 1753 |
2 |
| 1892 | |
3 |
|
| 1354 |
4 |
| 1384 | |
分析表中数据,你认为哪种方案制取氨气的效果最好?________![]() 填序号
填序号![]() ,该方案制取氨气效果好的可能原因是_______________。
,该方案制取氨气效果好的可能原因是_______________。
(2)装置D的作用是______________________________________。
(3)实验结束后,若测得干燥管C增重![]() ,装置E中气体的体积为
,装置E中气体的体积为![]() 已折算为标准状况
已折算为标准状况![]() ,则氨分子中氮、氢的原子个数比为___________
,则氨分子中氮、氢的原子个数比为___________![]() 用含m、V的代数式表示
用含m、V的代数式表示![]() ;若测量时,发现E装置中液面左低右高,则测得的比值___________
;若测量时,发现E装置中液面左低右高,则测得的比值___________![]() 填“偏大”“偏小”或“不变”
填“偏大”“偏小”或“不变”![]() 。
。