题目内容
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:X2(g)+3Y2(g) 2XY3(g) △H=-92.6kJ·mol-1
2XY3(g) △H=-92.6kJ·mol-1
起始时各物质物质的量如下表所示:
| 容器 编号 | 起始时各物质物质的量/mol | ||
| X2 | Y2 | XY3 | |
| ① | 1 | 3 | 0 |
| ② | 0.6 | 1.8 | 0.8 |
达到平衡后,①容器中XY3的物质的量为0.5mol。下列叙述正确的是
A.容器①、②中反应的平衡常数不相等
B.达平衡时,容器②中 XY3的物质的量浓度为2mol·L—1
C.容器①中反应达到平衡时放出的热量为23.15 kJ
D.容器②中反应达到平衡时放出热量
BC
解析试题分析:A、温度相同,平衡常数相同,错误;B、反应①②为等效平衡,达到同一个平衡状态,c(XY3)=0.5÷0.25=2mol·L—1,正确;C、列式为2:92.6=0.5:x x=23.15,正确;D、平衡时XY3的物质的量为0.5mol,故容器②应逆向进行,吸收热量,错误。
考点:考查化学平衡与反应热的有关问题。

练习册系列答案
相关题目
科学家正在研究开发新的能源,如核能、太阳能、风能、地热、潮汐热等。“绿色能源”是目前正在研究的新能源之一,把高粱、玉米等绿色植物的种子经发酵、蒸馏就可以得到“绿色能源”中的一种。这种物质是( )
| A.氢气 | B.甲烷 | C.酒精 | D.木炭 |
下列说法中正确的是
| A.在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B.生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,反应为吸热反应 |
| C.反应产物的总焓大于反应物的总焓时,反应吸热,ΔH>0 |
| D.ΔH的大小与热化学方程式的计量系数无关 |
金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石并需要吸收能量。已知12g石墨或金刚石完全燃烧时放出的热量依次为Q1和Q2,下列说法错误的是
| A.Q1< Q2 |
| B.石墨不如金刚石稳定 |
| C.质量相等的石墨与金刚石,石墨具有的能量比金刚石低 |
| D.质量相等的石墨与金刚石完全燃烧,生成的二氧化碳一样多 |
已知25℃、101kPa下,如图所示,石墨的燃烧热为393.5kJ/mol,金刚石的燃烧热为395.0kJ/mol 。下列说法或表达正确的是: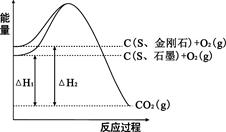
| A.金刚石比石墨稳定 |
| B.C(s、石墨)=C(s、金刚石)△H =+1.5kJ/mol |
| C.△H1<△H2 |
| D.如果使用催化剂,△H1和△H2都变小 |
“低碳经济,节能减排”是21世纪世界经济发展的新思路。”下列与之相悖的是( )
| A.开发水能、风能、太阳能、地热能、核能等新能源,减少使用煤、石油等化石燃料 |
| B.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |
| C.大力开采煤、石油和天然气,以满足经济发展的需要 |
| D.大力发展新能源汽车,如混合动力汽车、电动汽车等,以减少碳、氮氧化物的排放 |
下列有关化学反应能量变化的叙述一定正确的是
| A.生成物总能量大于反应物总能量,该反应为放热反应 |
| B.一个化学反应需要加热才能进行,该反应为吸热反应 |
| C.应用盖斯定律,可计算某些难以直接测量的化学反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件的?H不同 |