题目内容
【题目】铝鞣剂在皮革工业有广泛应用。某学习小组以铝灰为原料制备铝鞣剂[ Al(OH)2Cl],设计如下化工流程(提示:铝灰的主要成分是Al、Al2O3、AlN、FeO等):
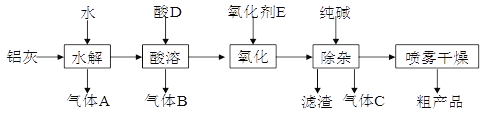
请回答下列问题:
(1)酸D的化学式为__________;气体C的电子式___________。
(2)实验室检验气体A的操作是________________;“水解”温度保持在90℃左右,写出水解生成A的化学方程式:________________________。
(3)“酸溶”温度控制在30℃~35℃,不宜太低,也不宜太高,其原因是_________________;氧化剂E宜选择_________(填字母)。
A.漂白液 | B.稀硝酸 | C.酸性高锰酸钾溶液 | D.溴水 |
(4)“除杂”过程中产生滤渣的离子方程式为_________________________。
(5)粗产品略显浅黄色,可能含有的杂质主要是_________________(填化学式)。
若用“蒸发”代替“喷雾干燥”,其后果是____________________________。
【答案】HCl ![]() 用镊子夹取一片湿润的红色石蕊试纸接触气体A,若试纸变蓝,则A为NH3(合理答案均计分)
用镊子夹取一片湿润的红色石蕊试纸接触气体A,若试纸变蓝,则A为NH3(合理答案均计分) ![]() 温度太低,反应慢;温度太高,盐酸挥发快(合理答案均计分) A 2Fe3++ 3CO32-+ 3H2O = 2Fe(OH)3↓+3CO2↑ Fe(OH)3(写任何形式的碱式氯化铁也计分) Al(OH)2Cl水解生成Al(OH)3,几乎得不到Al(OH)2Cl(或产率很低其他合理答案均计分)
温度太低,反应慢;温度太高,盐酸挥发快(合理答案均计分) A 2Fe3++ 3CO32-+ 3H2O = 2Fe(OH)3↓+3CO2↑ Fe(OH)3(写任何形式的碱式氯化铁也计分) Al(OH)2Cl水解生成Al(OH)3,几乎得不到Al(OH)2Cl(或产率很低其他合理答案均计分)
【解析】
铝灰主要成分为Al、Al2O3、AlN、FeO等,加入水发生反应,氮化铝和水反应生成氢氧化铝和氨气,即A为氨气,然后应加入盐酸溶解后,生成氯化铝溶液和氯化亚铁溶液,生成气体B为氢气,可加入漂白剂氧化亚铁离子为铁离子,加入纯碱调节溶液的pH使铁离子全部沉淀,生成气体C为二氧化碳,采用喷雾干燥制备铝鞣剂。
(1)由以上分析可知D为盐酸,气体C为二氧化碳,电子式为:![]() ;
;
(2)A为氨气,为碱性气体,可以用镊子夹取一片湿润的红色石蕊试纸接触气体A,若试纸变蓝,则A为NH3;氮化铝和水发生水解反应生成氢氧化铝和氨气,方程式为:![]() ;
;
(3)温度太低,反应慢;温度太高,盐酸挥发快,则酸溶温度控制在30℃~35℃,不宜太低或太高;漂白液的主要成分是NaClO和NaCl,其氧化Fe2+可生成Cl-,而稀硝酸、酸性高锰酸钾溶液、溴水氧化Fe2+都会有其他杂质离子生成,故只有A正确,选A;
(4)滤渣为氢氧化铁,可由铁离子与碳酸根离子水解生成,方程式为:2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑;
(5)产品含有氢氧化铁,可导致略显黄色,铝鞣剂主要成分为Al(OH)2Cl,在加热蒸发时会发生水解,为防止水解利用喷雾干燥,减少铝鞣剂水解;所以答案为:Al(OH)2Cl水解生成Al(OH)3,几乎得不到Al(OH)2Cl。

 阅读快车系列答案
阅读快车系列答案【题目】氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
(1)根据如图提供的信息,写出该反应的热化学方程式____________________________,下图的曲线中________(填“a” 或“b”)表示加入铁触媒(催化剂)的能量变化曲线。
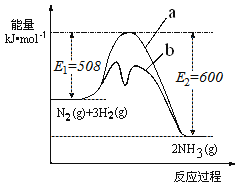
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是_____________。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n molN2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)500℃、50MPa时,在容积为1 L的容器中加入1 mol N2、3 mol H2,反应达平衡后测得平衡常数为K,此时N2的转化率为a。则K和a的关系是K=_______________。
(4)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) |
ⅰ | 450 |
| 1 |
ⅱ | ______ |
| 10 |
ⅲ | 480 | ______ | 10 |
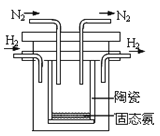
(5)1998年希腊亚里斯多德大学的两位科学家采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电解合成氨。其实验装置如图。阴极的电极反应式为________________________。