题目内容
〔化学—选修2:化学与技术〕(15分)
磷矿石主要以磷酸钙〔Ca3(PO4)2·H2O〕和磷灰石〔Ca3(OH)(PO4)3〕等形式存在。图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸。图(b)是热法磷酸生产过各中由磷灰石制单质磷的流程。

部分物质的相关性质如下:
| | 熔点/℃ | 沸点/℃ | 备注 |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 难溶于水,具有还原性 |
| SiF4 | -90 | -86 | 易水解 |
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的 ℅。
(2)以磷灰石为原料,湿法磷酸过程中Ca3F(PO4)3反应的化学方程式为: 。现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85℅的商品磷酸 吨。
(3)如图(b)所示,热法生产磷酸的第一步是将二氧化硅、过量焦炭与磷灰石混合,高温反应生成白磷。炉渣的主要成分是: (填化学式)冷凝塔1的主要沉积物是: 冷凝塔2的主要沉积物是:
(4)尾气中主要含有 ,还含有少量PH3、H2S和HF等,将尾气先通入纯碱溶液,可除去
再通入次氯酸钠溶液,可除去 (均填化学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是: 。
(1)69; (2) Ca3F(PO4)3+5H2SO4=3H3PO4+ 5CaSO4+HF↑;0.49;(3)CaSiO3;液态白磷;固态白磷;(4)SiF4、CO;SiF4、HF、 H2S ;PH3 (5)产品纯度大(浓度大)
解析试题分析:(1)根据图示可知生产含磷肥料,约占磷矿石使用量的比例是0.04+0.96×0.85×0.80="0.69." (2)以磷灰石为原料,用过量的硫酸溶解Ca3F(PO4)3,可制得磷酸。根据质量守恒定律可得反应的化学方程式为Ca3F(PO4)3+5H2SO4=3H3PO4+ 5CaSO4+HF↑;根据P守恒可得关系式 P2O5~2H3PO4.142份P2O52可制取196份的磷酸。1吨折合含有五氧化二磷约30%的磷灰石,含有P2O5的质量是0.3吨,所以可制取85℅的商品磷酸是质量是(196×0.3t)÷142÷0.85="0.49t;(3)" 二氧化硅、过量焦炭与磷灰石混合,在高温下反应除了得到白磷外,得到的难溶性的固体物质是CaSiO3;冷凝塔1的温度是70℃,280. 5℃>t>44℃所以此时主要沉积物是液态白磷;冷凝塔2的温度是12℃,低于白磷的熔点,故此时主要沉积物是固态白磷。(4)根据题目提供的信息,结合反应实际,在尾气中主要含有SiF4、CO,还含有少量PH3、H2S和HF等,将尾气先通入纯碱溶液, SiF4、HF、 H2S会与碳酸钠反应而除去;再通入次氯酸钠溶液,由于次氯酸钠有强氧化性,因此可除去有还原性的PH3 。(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高。但是产品纯度大,杂质少,因此逐渐被采用。
考点:考查磷矿石的主要用途、反应原理及有关计算的知识。

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案漂粉精常用于消毒游泳池中的水。有关漂粉精的叙述不正确的是
| A.生产原料是消石灰和氯气 | B.不宜长久储存 |
| C.有腐蚀及漂白作用 | D.消毒后无残渣,不会堵塞管道 |
硅是重要的半导体材料,构成了现代电子工业的基础。回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。
(2)硅主要以硅酸盐、 等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以 相结合,其晶胞中共有8个原子,其中在面心位置贡献 个原子。
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4CI在液氨介质中反应制得SiH4,该反应的化学方程式为 。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
| 键能(KJ/mol) | 356 | 413 | 336 | 226 | 318 | 452 |
②SiH4的稳定性小于CH4,更易生成氧化物,原因是 。
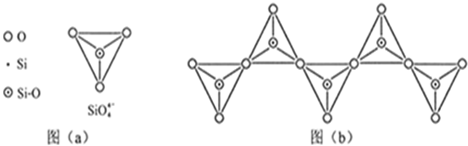
(6)在硅酸盐中,SiO44-四面体(如下图a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图b为一种无限长单链结构的多硅酸根;其中Si原子的杂化形式为 。Si与O的原子数之比为 化学式为 。
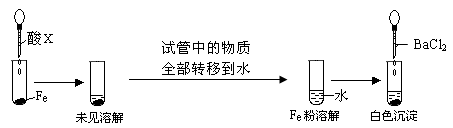
下表是实验室制备气体的有关内容:
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制氧气 | H2O2―→O2 | |
| ② | 制氨气 | NH4Cl―→NH3 | |
| ③ | 是氯气 | HCl―→Cl2 | |
(1)上表气体中:从制备过程看,必须选择合适的氧化剂才能实现的是________(填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是________。
(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中。

(3)若用上述制备O2的装置制备NH3,则选择的试剂为________________。
(4)制备Cl2需用8 mol·L-1的盐酸100 mL,现用12 mol·L-1的盐酸来配制。
①为提高配制的精确度,量取浓盐酸的仪器可选用下列中的________(填序号):

②配制过程中,除上图所列仪器外,还需要的仪器有________、________、________。
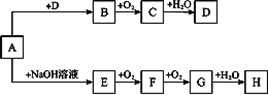

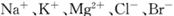 等离子)可提取溴,其生产流程如下:
等离子)可提取溴,其生产流程如下: