题目内容
2. 某学生用胆矾制取氧化铜固体,并研究氧化铜能否在氯酸钾受热分解实验中起催化作用.实验步骤如下:
某学生用胆矾制取氧化铜固体,并研究氧化铜能否在氯酸钾受热分解实验中起催化作用.实验步骤如下:①称量a g胆矾固体放入烧杯中,加水制成溶液,
向其中滴加氢氧化钠溶液至沉淀完全;
②把步骤①中的溶液和沉淀转移至蒸发皿中,加热
至溶液中的沉淀全变成黑色氧化铜为止;
③过滤、洗涤、干燥,称量所得固体质量为b g;
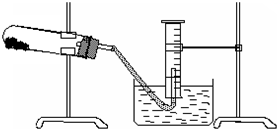
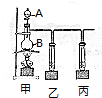
④取一定质量的上述氧化铜固体和一定质量的氯酸钾固体,混合均匀后加热,收集反应生成的氧气,如上图所示.请回答下列问题:
(1)上述各步操作中,需要用到玻璃棒的是①②③④(填写前面所述实验步骤的序号).
(2)由胆矾制备氧化铜的产率(实际产量与理论产量的百分比)为$\frac{25b}{8a}$×100%.
(3)为保证Cu2+沉淀完全,步骤①中溶液的pH应大于10.简述测定溶液pH的操作:把一小块pH试纸放在表面皿(或玻璃片)上,用蘸有混合溶液的玻璃棒点在试纸的中部,试纸变色后,试纸变色后,与标准比色卡比较来确定溶液的pH.
(4)为证明氧化铜在氯酸钾的分解反应中起催化作用,在上述实验①~④后还应该进行的实验操作是cadbe(按实验先后顺序填写字母序号).
a 过滤 b 烘干 c 溶解 d 洗涤 e 称量
(5)但有同学认为,还必须另外再设计一个实验才能证明氧化铜在氯酸钾受热分解的实验中起催化作用.你认为还应该进行的另一个实验是对比实验,称取相等质量的氯酸钾,加热,比较产生相同体积氧气所需的时间,或比较在相同时间内产生氧气的体积.
分析 (1)胆矾固体放入烧杯中,加水制成溶液时需要用玻璃棒搅拌,加速胆矾固体溶解速度;在蒸发时用玻璃棒搅拌,是为了防止局部温度过高使液滴飞溅;过滤时用到玻璃棒的作用是引流;氧化铜固体和一定质量的氯酸钾固体,混合均匀也需要玻璃棒的搅拌;
(2)ag胆矾中含铜元素质量为ag×$\frac{64}{250}$=$\frac{32}{125}$a,设能制得氧化铜的质量为X,根据铜守恒由X×$\frac{64}{80}$=$\frac{32}{125}$a,解得X=$\frac{8}{25}$a,据此计算由胆矾制备氧化铜的产率;
(3)根据pH试纸的使用方法答题;
(4)由于需要证明反应前后氧化铜的质量不变,反应后先将氧化铜从混合物中分离出来:加水溶解,进行过滤,得到的氧化铜上有氯化钾溶液,进行洗涤干燥,再进行称量即可;
(5)通过对比实验才能说明氧化铜的确加快了氯酸钾的反应速度,另取相同质量的氯酸钾固体,不加氧化铜直接加热,对比放出氧气的速率快慢,现象很明显;
解答 解:(1)胆矾固体放入烧杯中,加水制成溶液时需要用玻璃棒搅拌,加速胆矾固体溶解速度;在蒸发时用玻璃棒搅拌,是为了防止局部温度过高使液滴飞溅;过滤时用到玻璃棒的作用是引流;氧化铜固体和一定质量的氯酸钾固体,混合均匀也需要玻璃棒的搅拌,所以选择①②③④,
故答案为:①②③④;
(2)ag胆矾中含铜元素质量为ag×$\frac{64}{250}$=$\frac{32}{125}$a,设能制得氧化铜的质量为X,根据铜守恒由X×$\frac{64}{80}$=$\frac{32}{125}$a,解得X=$\frac{8}{25}$a,所以由胆矾制备氧化铜的产率:$\frac{b}{\frac{8}{25}a}$×100%=$\frac{25b}{8a}$×100%,
故答案为:$\frac{25b}{8a}$;
(3)测定溶液pH的操作为:把一小块pH试纸放在表面皿(或玻璃片)上,用蘸有混合溶液的玻璃棒点在试纸的中部,试纸变色后,试纸变色后,与标准比色卡比较来确定溶液的pH,
故答案为:把一小块pH试纸放在表面皿(或玻璃片)上,用蘸有混合溶液的玻璃棒点在试纸的中部,试纸变色后,试纸变色后,与标准比色卡比较来确定溶液的pH;
(4)由于需要证明反应前后氧化铜的质量不变,反应后先将氧化铜从混合物中分离出来:加水溶解,进行过滤,得到的氧化铜上有氯化钾溶液,进行洗涤干燥,再进行称量,
故答案为:cadbe;
(5)通过对比实验才能说明氧化铜的确加快了氯酸钾的反应速度,另取相同质量的氯酸钾固体,不加氧化铜直接加热,对比放出氧气的速率快慢,现象很明显,
故答案为:对比实验,称取相等质量的氯酸钾,加热,比较产生相同体积氧气所需的时间,或比较在相同时间内产生氧气的体积.
点评 本题主要考查物质的制备,难度不大,涉及产率计算、实验原理分析、实验基本操作、实验方案的设计等,注意基础知识的掌握和灵活运用.

| A. | 基态铜原子的价电子排布图: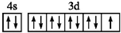 | |
| B. | CO2分子立体结构模型: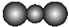 | |
| C. | 三氟化硼的电子式: | |
| D. | 35Br基态原子的电子排布式可简写为[Ar]4s24p5 |
A.饱和食盐水 B.水 C.浓H2SO4 D.碱石灰 E.铝粉 F.二氧化锰 G.浓盐酸 H.烧碱溶液
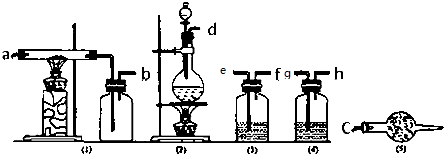
回答下列问题:(1)写出AlCl3露置在空气中生成白雾的化学方程式:AlCl3+3H2O?Al(OH)3+3HCl.
(2)从上述仪器中选取若干连成一制备并保存无水AlCl3的装置,用图中各管口标号按先后可连接为:d接e,f接g,h接a,b接c.
(3)填写连接装置中各选用仪器里应盛放的物质:
| 仪器标号 | (1) | (2)(上) | (2)(下) | (3) | (4) | (5) |
| 试剂标号 | G | F |
 (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2
在不同温度时K1、K2的值如表:
| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
②能判断恒温恒容容器CO2(g)+H2(g)?CO(g)+H2O(g)达到化学平衡状态的依据是B(填序号).
A.容器中压强不变 B.混合气体中c(CO)不变 C.容器中密度不变 D.c(CO)=c(CO2)
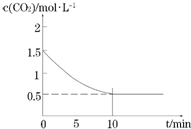
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)?FeO(s)+CO(g),CO2的浓度与时间的关系如图所示:
①该条件下反应的平衡常数为2;0-10min的平均反应速率v(CO)=0.1mol•L-1•min-1;
若铁粉足量,CO2的起始浓度为2.0mol•L-1,则平衡时CO2的浓度为0.67mol•L-1.
②下列措施中能使平衡时$\frac{c(CO)}{c(C{O}_{2})}$增大的是A(填序号)
A.升高温度 B.增大压强 C.充入一定量的CO2D.再加入一定量铁粉.
 某学习小组为探究部分元素化合物的性质,设计了下面的实验装置:
某学习小组为探究部分元素化合物的性质,设计了下面的实验装置: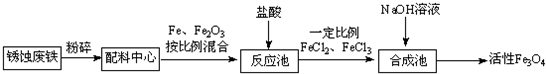
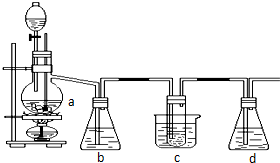 1、2-二溴乙烷可作汽油抗爆剂,常温下它是无色液体,密度2.18g/cm3,沸点131.4 0C,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室可以用下图所示装置制备1、2-二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管c中装有浓溴水.
1、2-二溴乙烷可作汽油抗爆剂,常温下它是无色液体,密度2.18g/cm3,沸点131.4 0C,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室可以用下图所示装置制备1、2-二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管c中装有浓溴水.