题目内容
【题目】实验表明:将氯水滴加到一片蓝色石蕊试纸上,会出现如图所示的半径慢慢扩大的内外两个圆环,且两环颜色不同,下列有关说法中不正确的是( )
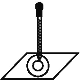
A.此实验表明氯水有酸性、漂白性
B.内环呈白色,外环呈红色或浅红色
C.内外环上颜色的差异表明此变化过程中,盐酸与指示剂的反应比氧化还原反应快
D.氯水中形成次氯酸的反应中还原产物是HClO
【答案】D
【解析】
A. 此实验表明氯水有酸性、漂白性,而且先表现出酸性,后表现出氧化强,A正确;
B. 内环是次氯酸将红色物质漂白、呈白色,外环是酸使酚酞呈红色或浅红色,B正确;
C. 内外环上颜色的差异表明此变化过程中,盐酸先与指示剂反应,次氯酸后与指示剂发生氧化还原反应,C正确;
D. 氯水中形成次氯酸的反应中氧化产物是HClO,D错误。
故选D。

练习册系列答案
相关题目