题目内容
【题目】烃A中碳、氢两种元素的质量比是24:5,G具有浓郁的香味。它们之间的转化关系如下(含有相同官能团的有机物通常具有相似的化学性质):
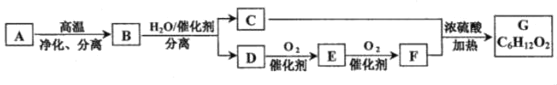
请回答:
(1)化合物B所含的官能团的名称是___。
(2)D的结构简式是___。
(3)C+F→G的化学方程式是___。
(4)下列说法正确的是___。
A.在工业上,A→B的过程可以获得汽油等轻质油
B.有机物C与D都能与金属钠反应,C经氧化也可得到F
C.可以用碳酸钠溶液鉴别E、F、G
D.等质量的E、G混合物,无论以何比例混合,完全燃烧耗氧量相同
【答案】碳碳双键 CH3CH2CH2OH H3CH2COOH+CH3CHOHCH3![]() CH3CH2COOCH(CH3)2+H2O CD
CH3CH2COOCH(CH3)2+H2O CD
【解析】
烃A中碳、氢两种元素的质量比是24:5,则N(C):N(H)=![]() ,应为C4H10,由生成物G的分子式可知C为CH3CHOHCH3,D为CH3CH2CH2OH,E为CH3CH2CHO,F为CH3CH2COOH,B为CH3CH=CH2,生成G为CH3CH2COOCH(CH3)2,以此解答该题。
,应为C4H10,由生成物G的分子式可知C为CH3CHOHCH3,D为CH3CH2CH2OH,E为CH3CH2CHO,F为CH3CH2COOH,B为CH3CH=CH2,生成G为CH3CH2COOCH(CH3)2,以此解答该题。
(1)B为CH3CH=CH2,含有的官能团为碳碳双键,故答案为:碳碳双键;
(2)D为CH3CH2CH2OH,故答案为:CH3CH2CH2OH;
(3) C+F→G的化学方程式是CH3CH2COOH+CH3CHOHCH3![]() CH3CH2COOCH(CH3)2+H2O,
CH3CH2COOCH(CH3)2+H2O,
故答案为:CH3CH2COOH+CH3CHOHCH3![]() CH3CH2COOCH(CH3)2+H2O;
CH3CH2COOCH(CH3)2+H2O;
(4)A.在工业上,A→B的过程为裂解,可获得乙烯等烯烃,而裂化可以获得汽油等轻质油,故A错误;
B.有机物C与D都能与金属钠反应,C经氧化生成丙酮,故B错误;
C.醛可溶于水,酸与碳酸钠反应,酯类不溶于水,则可以用碳酸钠溶液鉴别E、F、G,故C正确;
D.E、G的最简式相同,则等质量的E、G混合物,无论以何比例混合,完全燃烧耗氧量相同,故D正确;故答案为:CD。

【题目】Bodensteins研究了下列反应:2HI(g)![]() H2(g)+I2(g)
H2(g)+I2(g)![]() 。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示。当升高温度,再次达到平衡时,v正 v逆可能落在A、B、C、D、E哪些点。
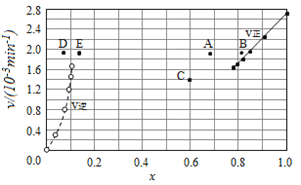
A. A D B. B D C. B E D. A E

