题目内容
下表是某些原子晶体的熔点和硬度
原子晶体 | 金刚石 | 氮化硼 | 碳化硅 | 石英 | 硅 | 锗 |
熔点/℃ | 3 900 | 3 000 | 2 700 | 1 710 | 1 410 | 1 211 |
硬度 | 10 | 9.5 | 9.5 | 7 | 6.5 | 6.0 |
分析表中的数据,判断下列叙述正确的是( )。
①构成原子晶体的原子种类越多,晶体的熔点越高
②构成原子晶体的原子间的共价键键能越大,晶体的熔点越高
③构成原子晶体的原子的半径越大,晶体的硬度越大
④构成原子晶体的原子的半径越小,晶体的硬度越大
A.①② B.③④ C.①③ D.②④
D
【解析】原子晶体的熔点和硬度与构成原子晶体的原子间的共价键键能有关,而原子间的共价键键能与原子半径的大小有关。

 名校课堂系列答案
名校课堂系列答案下图为元素周期表前4周期的一部分,下列有关R、W、X、Y、Z 5种元素的叙述中,正确的是( )。
|
|
|
|
X |
|
|
|
W | Y |
| R |
|
| Z |
|
A.W、R元素单质分子内的化学键都是非极性键
B.X、Z元素都能够形成双原子分子
C.键能W—H>Y—H,键的极性Y—H>W—H
D.键长X—H<W—H,键能X—H<W—H
下表列出了3种燃煤烟气脱硫方法的原理。
方法Ⅰ | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
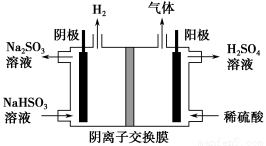
方法Ⅲ | 用Na2SO3溶液吸收SO2,再经电解转化为H2SO4 |
(1)方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:
2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3
能提高燃煤烟气中SO2去除率的措施有________(填字母)。
A.增大氨水浓度
B.升高反应温度
C.使燃煤烟气与氨水充分接触
D.通入空气使HSO3-转化为SO42-
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是____________(用离子方程式表示)。
(2)方法Ⅱ中主要发生了下列反应:
2CO(g)+SO2(g)=S(g)+2CO2(g) ΔH=8.0 kJ·mol-1
2H2(g)+SO2(g)=S(g)+2H2O(g) ΔH=90.4 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) ΔH=-566.0 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1
S(g)与O2(g)反应生成SO2(g)的热化学方程式可表示为________。
(3)方法Ⅲ中用惰性电极电解NaHSO3溶液的装置如下图所示。阳极区放出气体的成分为________(填化学式)。