��Ŀ����
ŷ��ԭ����2012��1��1�������պ���̼��˰��Ӧ�Ա����ڻ���ȫ���ů��ʹ�ö���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������̼��Դ���о��Եø��ӽ��ȣ������û�ѧ��Ӧԭ�������֪ʶ�о�̼���仯���������
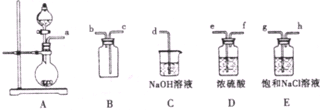
��1���õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ɸ÷�Ӧ�Ļ�ѧ����ʽ����ϵ����˳�����ڴ�����ϣ��õ����ű������ת�Ƶķ������Ŀ��
C+ KMnO4+ H2SO4�� CO2��+ MnSO4+ K2SO4+ H2O
��2����̿��������ȡˮú�������12g̼��ˮ������ȫ��Ӧ����ˮú��ʱ��������131.6kJ�������÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��3������̿�ɴ���������Ⱦ��NO����2L�ܱ������м���NO�ͻ���̿�������ʣ�����������E��F�����¶ȷֱ���T1��T2ʱ����ø�����ƽ��ʱ���ʵ������±���
�������ϱ����ݣ�д��NO�����̿��Ӧ�Ļ�ѧ����ʽ ��
�ڸ���������Ϣ�жϣ��¶�T1��T2�Ĺ�ϵ�ǣ�����ţ� ��
a��T1��T2 b��T1��T2 c�����Ƚ�
��4����״���£���4.48L CO2ͨ��200mL 1.5mol/L��NaOH��Һ��������Һ�и�����Ũ���ɴ�С��˳��Ϊ ��
��5��CO����������ȼ�ϵ�ص�ȼ�ϣ�ij������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ��õ����Li2CO3��Na2CO3�������λ����������ʣ�COΪ����ȼ����������CO2�Ļ����Ϊ������ȼ�����Ƶ���650���¹�����ȼ�ϵ�أ��为����Ӧʽ��2CO+2CO32--4e-=4CO2��������Ӧʽ�� ������ܷ�Ӧʽ�� ��
��6��CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2.8��10-9��CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10-4mo1/L�������ɳ�������CaCl2��Һ����СŨ��Ϊ ��
��7�����³�ѹ�£�����CO2ˮ��Һ��pH=5.6��c��H2CO3��=1.5��10-5mol/L��������ˮ�ĵ��뼰H2CO3�ĵڶ������룬��H2CO3?HCO3-+H+�ĵ���ƽ�ⳣ��K= ������֪��10-5.6=2.5��10-6����
��1���õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ɸ÷�Ӧ�Ļ�ѧ����ʽ����ϵ����˳�����ڴ�����ϣ��õ����ű������ת�Ƶķ������Ŀ��
��2����̿��������ȡˮú�������12g̼��ˮ������ȫ��Ӧ����ˮú��ʱ��������131.6kJ�������÷�Ӧ���Ȼ�ѧ����ʽΪ
��3������̿�ɴ���������Ⱦ��NO����2L�ܱ������м���NO�ͻ���̿�������ʣ�����������E��F�����¶ȷֱ���T1��T2ʱ����ø�����ƽ��ʱ���ʵ������±���
���� T/��n/mol | ����̿ | NO | E | F |
| ��ʼ | 2.030 | 0.100 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
�ڸ���������Ϣ�жϣ��¶�T1��T2�Ĺ�ϵ�ǣ�����ţ�
a��T1��T2 b��T1��T2 c�����Ƚ�
��4����״���£���4.48L CO2ͨ��200mL 1.5mol/L��NaOH��Һ��������Һ�и�����Ũ���ɴ�С��˳��Ϊ
��5��CO����������ȼ�ϵ�ص�ȼ�ϣ�ij������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ��õ����Li2CO3��Na2CO3�������λ����������ʣ�COΪ����ȼ����������CO2�Ļ����Ϊ������ȼ�����Ƶ���650���¹�����ȼ�ϵ�أ��为����Ӧʽ��2CO+2CO32--4e-=4CO2��������Ӧʽ��
��6��CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2.8��10-9��CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10-4mo1/L�������ɳ�������CaCl2��Һ����СŨ��Ϊ
��7�����³�ѹ�£�����CO2ˮ��Һ��pH=5.6��c��H2CO3��=1.5��10-5mol/L��������ˮ�ĵ��뼰H2CO3�ĵڶ������룬��H2CO3?HCO3-+H+�ĵ���ƽ�ⳣ��K=
���㣺������ԭ��Ӧ,�Ȼ�ѧ����ʽ,��ѧ��Դ���͵��,���������ˮ��Һ�еĵ���ƽ��
ר�⣺�����������������
��������1������������ԭ��Ӧ�е�ʧ��������Ⱥ�ԭ���غ�����ƽ��ѧ����ʽ��
��2��12gC�����ʵ�����1mol��1molC��ˮ������Ӧ������131.6kJ������
��3�����ɱ������ݿ�֪��C��NO��E��F�Ļ�ѧ������֮��Ϊ0.03��0.06��0.03��0.03=1��2��1��1����Ӧ��C�����������ԭ���غ��֪������ΪN2��CO2��
���ɱ������ݿ�֪���¶���T1��ΪT2��ƽ�����淴Ӧ�ƶ�����������Ӧ�����ȣ����Ƿ��Ȳ�ȷ���������ж��¶ȱ仯��
��4��n ��CO2��=0.2mol��n��NaOH��=0.3mol����Ӧ�Ŀ��ܷ���ʽ�У�CO2+2NaOH=Na2CO3+H2O��CO2+NaOH=NaHCO3��1��n��NaOH����n ��CO2����2��������Һ�е�������̼���ơ�̼�����ƣ������ò����к�Na2CO3Ϊxmol��NaHCO3Ϊymol��
��÷����飺
��ã�x=0.1��y=0.1��
��Һ�е�����Ϊ�����ʵ�����̼���ƺ�̼�����ƣ�̼���ˮ��̶ȴ���̼��������ӣ�
��5��ȼ�ϵ���У�������ȼ��ʧ���ӷ���������Ӧ���������������õ��ӷ�����ԭ��Ӧ����ʧ�������ʱ���������缫��Ӧʽ��Ӽ��õ�ط�Ӧʽ��
��6�������ܶȻ����������Ȼ���Ũ�ȣ�
��7��K=
��
��2��12gC�����ʵ�����1mol��1molC��ˮ������Ӧ������131.6kJ������
��3�����ɱ������ݿ�֪��C��NO��E��F�Ļ�ѧ������֮��Ϊ0.03��0.06��0.03��0.03=1��2��1��1����Ӧ��C�����������ԭ���غ��֪������ΪN2��CO2��
���ɱ������ݿ�֪���¶���T1��ΪT2��ƽ�����淴Ӧ�ƶ�����������Ӧ�����ȣ����Ƿ��Ȳ�ȷ���������ж��¶ȱ仯��
��4��n ��CO2��=0.2mol��n��NaOH��=0.3mol����Ӧ�Ŀ��ܷ���ʽ�У�CO2+2NaOH=Na2CO3+H2O��CO2+NaOH=NaHCO3��1��n��NaOH����n ��CO2����2��������Һ�е�������̼���ơ�̼�����ƣ������ò����к�Na2CO3Ϊxmol��NaHCO3Ϊymol��
��÷����飺
|
��Һ�е�����Ϊ�����ʵ�����̼���ƺ�̼�����ƣ�̼���ˮ��̶ȴ���̼��������ӣ�
��5��ȼ�ϵ���У�������ȼ��ʧ���ӷ���������Ӧ���������������õ��ӷ�����ԭ��Ӧ����ʧ�������ʱ���������缫��Ӧʽ��Ӽ��õ�ط�Ӧʽ��
��6�������ܶȻ����������Ȼ���Ũ�ȣ�
��7��K=
| c(H+)��c(HCO3-) |
| c(H2CO3) |
���
�⣺��1�������������Ԫ�ػ��ϼ۽���7-2=5�ۣ�̼Ԫ�ػ��ϼ�����4-0=4�ۣ����ϼ�������=���ϼ۽����������Ը������ǰ��ϵ����4��̼����ǰ��ϵ����5������ԭ���غ㣬������̼ǰ��5��������ǰ��4�������ǰ����2������������غ㣬��������ǰ����6������ԭ�Ӻ���ԭ���غ㣬����Ϊ6��ˮ���ӣ��÷�Ӧ��ת�Ƶ�����Ϊ20��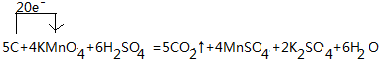 ��
��
�ʴ�Ϊ��5��4��6��5��4��2��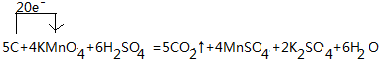 ��
��
��2��12gC�����ʵ�����1mol��1molC��ˮ������Ӧ������131.6kJ���������Ȼ�ѧ��Ӧ����ʽΪC��s��+H2O��g��=CO��g��+H2��g����H=+131.6 kJ?mol-1��
�ʴ�Ϊ��C��s��+H2O��g��=CO��g��+H2��g����H=+131.6 kJ?mol-1��
��3�����ɱ������ݿ�֪��C��NO��E��F�Ļ�ѧ������֮��Ϊ0.03��0.06��0.03��0.03=1��2��1��1����Ӧ��C�����������ԭ���غ��֪������ΪN2��CO2���Ҹ÷�ӦΪ���淴Ӧ���ʷ�Ӧ����ʽΪ��C+2NO?N2+CO2��
�ʴ�Ϊ��C+2NO?N2+CO2��
���ɱ������ݿ�֪���¶���T1��ΪT2��ƽ�����淴Ӧ�ƶ�����������Ӧ�����ȣ����Ƿ��Ȳ�ȷ�������ж��¶ȱ仯���ʴ�Ϊ��c��
��4��n ��CO2��=0.2mol��n��NaOH��=0.3mol����Ӧ�Ŀ��ܷ���ʽ�У�CO2+2NaOH=Na2CO3+H2O��CO2+NaOH=NaHCO3��1��n��NaOH����n ��CO2����2��������Һ�е�������̼���ơ�̼�����ƣ������ò����к�Na2CO3Ϊxmol��NaHCO3Ϊymol��
��÷����飺
��ã�x=0.1��y=0.1��
�ں������ʵ�����̼���ơ�̼�����Ƶ���Һ�У�c��Na+�����̼�������ˮ�����̼��������ӵ�ˮ�⣬��c��HCO3-����c��CO32-����
ˮ��ʹ��Һ�Լ��ԣ���c��OH-����c��H+�����������Ӵ����������ӣ�����c��HCO3-����c��CO32-����c��OH-����c��H+����
������Ũ�ȴ�СΪc��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+����
�ʴ�Ϊ��c��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+����
��5����ȼ�ϵ���У������ϵ缫��ӦʽΪ2CO+2CO32--4e-=4CO2�������������õ��ӺͶ�����̼��Ӧ����̼������ӣ��缫��ӦʽΪO2+2CO2+4e-=2 CO32-�����ط�ӦʽΪ2CO+O2=2CO2���ʴ�Ϊ��O2+2CO2+4e-=2 CO32-��2CO+O2=2CO2��
��6�������Һ��̼�������Ũ��Ϊ1��10-4mo1/L�������Һ��c��Ca 2+ ��=
=
mol/L=2.8��10-5mo1/L����ԭ����Һ��c��CaCl2��=5.6��10-5mo1/L���ʴ�Ϊ��5.6��10-5mo1/L��
��7��K=
=
=4.17��10-7���ʴ�Ϊ��4.17��10-7��
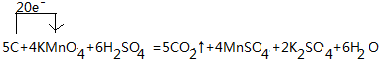 ��
���ʴ�Ϊ��5��4��6��5��4��2��
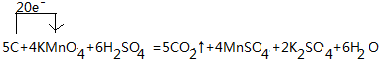 ��
����2��12gC�����ʵ�����1mol��1molC��ˮ������Ӧ������131.6kJ���������Ȼ�ѧ��Ӧ����ʽΪC��s��+H2O��g��=CO��g��+H2��g����H=+131.6 kJ?mol-1��
�ʴ�Ϊ��C��s��+H2O��g��=CO��g��+H2��g����H=+131.6 kJ?mol-1��
��3�����ɱ������ݿ�֪��C��NO��E��F�Ļ�ѧ������֮��Ϊ0.03��0.06��0.03��0.03=1��2��1��1����Ӧ��C�����������ԭ���غ��֪������ΪN2��CO2���Ҹ÷�ӦΪ���淴Ӧ���ʷ�Ӧ����ʽΪ��C+2NO?N2+CO2��
�ʴ�Ϊ��C+2NO?N2+CO2��
���ɱ������ݿ�֪���¶���T1��ΪT2��ƽ�����淴Ӧ�ƶ�����������Ӧ�����ȣ����Ƿ��Ȳ�ȷ�������ж��¶ȱ仯���ʴ�Ϊ��c��
��4��n ��CO2��=0.2mol��n��NaOH��=0.3mol����Ӧ�Ŀ��ܷ���ʽ�У�CO2+2NaOH=Na2CO3+H2O��CO2+NaOH=NaHCO3��1��n��NaOH����n ��CO2����2��������Һ�е�������̼���ơ�̼�����ƣ������ò����к�Na2CO3Ϊxmol��NaHCO3Ϊymol��
��÷����飺
|
�ں������ʵ�����̼���ơ�̼�����Ƶ���Һ�У�c��Na+�����̼�������ˮ�����̼��������ӵ�ˮ�⣬��c��HCO3-����c��CO32-����
ˮ��ʹ��Һ�Լ��ԣ���c��OH-����c��H+�����������Ӵ����������ӣ�����c��HCO3-����c��CO32-����c��OH-����c��H+����
������Ũ�ȴ�СΪc��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+����
�ʴ�Ϊ��c��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+����
��5����ȼ�ϵ���У������ϵ缫��ӦʽΪ2CO+2CO32--4e-=4CO2�������������õ��ӺͶ�����̼��Ӧ����̼������ӣ��缫��ӦʽΪO2+2CO2+4e-=2 CO32-�����ط�ӦʽΪ2CO+O2=2CO2���ʴ�Ϊ��O2+2CO2+4e-=2 CO32-��2CO+O2=2CO2��
��6�������Һ��̼�������Ũ��Ϊ1��10-4mo1/L�������Һ��c��Ca 2+ ��=
| Ksp |
| c(CO32-) |
| 2.8��10-9 |
| 1��10-4 |
��7��K=
| c(H+)��c(HCO3-) |
| c(H2CO3) |
| 10-5.6��10-5.6 |
| 1.5��10-5 |
���������⿼����ۺϣ��漰ƽ�ⳣ�����йؼ��㡢����Ũ�ȴ�С�Ƚϡ�ԭ���ԭ�����Ȼ�ѧ��Ӧ��������ԭ��Ӧ��֪ʶ�㣬��Щ֪ʶ�㶼�ǿ����ȵ㣬���ݻ�����ʽ����Һ�е����ʼ��غ�˼�롢ԭ���ԭ����֪ʶ��������ע�⣨6����������Һ���ʱ������Ũ�Ƚ�Ϊԭ����һ�룬Ϊ�״��㣮

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
���г�ȥ���ʵ�ʵ�鷽����ȷ���ǣ�������
| A����ȥCO������O2��ͨ�����ȵ�Cu�����ռ����� |
| B����ȥK2CO3����������NaHCO3�����������м��� |
| C����ȥKCl��Һ�е�����MgCl2����������NaOH��Һ������ |
| D����ȥCO2�е�����HCl��ͨ�뱥��NaHCO3��Һ���ռ����� |
NA��ʾ�����ӵ�������������������ȷ���ǣ�������
| A��1mol Na2O��Na2O2�Ļ������������������ΪNA |
| B��1.7g H2O2�к��еĵ�����Ϊ0.9NA |
| C��1mol Na2O2��������CO2��Ӧ������ת����Ϊ2NA |
| D����״���£�2.24L CO2��CO������������Ϊ0.1NA |