题目内容
3.下列各组中的离子,能在溶液中大量共存的是( )| A. | H+、Na+、CO32-、Cl- | B. | Ba2+、Na+、NO3-、Cl- | ||
| C. | K+、Ba2+、SO42-、Cl- | D. | Ag+、Al3+、Cl-、OH- |
分析 A.氢离子与碳酸根离子反应;
B.四种离子之间不满足离子反应发生条件;
C.钡离子与硫酸根离子反应生成硫酸钡沉淀;
D.银离子、铝离子与氢氧根离子反应.
解答 解:A.H+、CO32-之间发生反应,在溶液中不能大量共存,故A错误;
B.Ba2+、Na+、NO3-、Cl-之间不发生反应,在溶液中能够大量共存,故B正确;
C.Ba2+、SO42-之间反应生成硫酸钡沉淀,在溶液中不能大量共存,故C错误;
D.Ag+、Al3+、都与OH-发生反应,在溶液中不能大量共存,故D错误;
故选B
点评 本题考查离子共存的正误判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.下列离子方程式正确的是( )
| A. | 铁粉加入三氯化铁溶液中:Fe+2Fe3+═3Fe2+ | |
| B. | 钠与水的反应Na+2H2O═Na++2OH -+H2↑ | |
| C. | 铜片插入硝酸银溶液中Cu+Ag+═Cu2++Ag | |
| D. | 大理石溶于醋酸的反应CaCO3+2H+═Ca2++CO2↑+H2O |
18.下列反应的离子方程式正确的是( )
| A. | 钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 氢氧化铝中和胃酸:Al(OH)3+3H+═Al3++3H2O | |
| D. | 用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ |
12.如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )


| A. | 两条曲线间任意点均有c(H+)×c(OH-)=KW | |
| B. | XZ线上任意点均有pH=7 | |
| C. | 图中T1<T2 | |
| D. | M区域内任意点均有c(H+)<c(OH-) |
20.下列表达正确的是( )
| A. | HClO的电子式为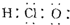 | |
| B. | H2S的电子式可表示为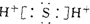 | |
| C. | 用电子式表示Na2O的形成过程为2Nax+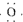 →2Na+ →2Na+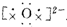 | |
| D. | MgCl2的电子式为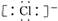 Mg2+ Mg2+ |
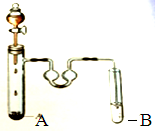 如图是制取溴苯的装置,试回答:
如图是制取溴苯的装置,试回答: