题目内容
【题目】金属钛(Ti)是一种具有许多优良性能的金属,钛和钛合金被认为是21世纪的重要金属材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态电子排布式可表示为_____。
②与BH4-互为等电子体的阳离子的化学式为_____。
③H、B、Ti原子的第一电离能由小到大的顺序为_____。
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。
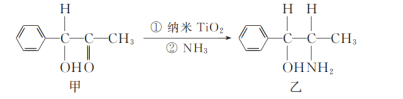
化合物乙的分子中采取sp3杂化方式的原子个数为_____。
(3)水溶液中并没有[Ti(H2O)6)]4+离子,而是[Ti(OH)2(H2O)4]2+离子,1mol[Ti(OH)2(H2O)4]2+中σ键的数目为____。
(4)氮化钛(TiN)具有典型的NaCl型结构,某碳氮化钛化合物,结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,则此碳氮化钛化合物的化学式是_____。
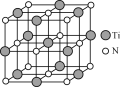
【答案】1s22s22p62s23p63d2或[Ar]3d2 NH4+ Ti<B<H 5 16mol Ti4CN3
【解析】
(1)①钛是22号元素,Ti2+核外有20个电子;②BH4-含有5个原子,价电子总数为8,据此分析书写与BH4-互为等电子体的阳离子;③根据第一电离能的变化规律分析判断H、B、Ti原子的第一电离能的大小顺序;
(2)采取sp3杂化方式的原子的价层电子对数=4,据此分析判断分子中采取sp3杂化方式的原子个数;
(3) 配位键属于σ键,1个单键为1个σ键,据此分析判断;
(4)根据均摊法计算晶胞中碳、氮、钛原子数目,进而确定化学式。
(1)①钛是22号元素,Ti2+核外有20个电子,根据构造原理知其基态核外电子排布式为:1s22s22p63s23p63d2,故答案为:1s22s22p63s23p63d2;
②BH4-含有5个原子,价电子总数为8,与BH4-互为等电子体的阳离子为NH4+,故答案为:NH4+;
③同一周期,从左到右,元素的第一电离能呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素。同族元素,从上至下第一电离能逐渐减小,金属元素的第一电离能小于非金属元素,H、B、Ti原子的第一电离能由小到大的顺序为Ti<B<H,故答案为:Ti<B<H;
(2)化合物乙(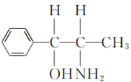 )的分子中采取sp3杂化方式的原子个数有
)的分子中采取sp3杂化方式的原子个数有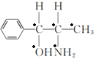 (标记为●的原子采取sp3杂化),共5个,故答案为:5;
(标记为●的原子采取sp3杂化),共5个,故答案为:5;
(3) 1个[Ti(OH)2(H2O)4]2+中含有6个配位键,10个O-H,因此1mol[Ti(OH)2(H2O)4]2+中含有σ键的数目为16mol,故答案为:16mol;
(4) 某碳氮化钛化合物,结构是用碳原子取代氮化钛晶胞顶点的氮原子,利用均摊法可知,晶胞中含有碳原子数为8×![]() =1,含有氮原子数为6×
=1,含有氮原子数为6×![]() =3,含有钛原子数为12×
=3,含有钛原子数为12×![]() +1=4,所以碳、氮、钛原子数之比为1∶3∶4,则该化合物的化学式为Ti4CN3,故答案为:Ti4CN3。
+1=4,所以碳、氮、钛原子数之比为1∶3∶4,则该化合物的化学式为Ti4CN3,故答案为:Ti4CN3。

 名校课堂系列答案
名校课堂系列答案【题目】FeCl3在现代工业生产中应用广泛.某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
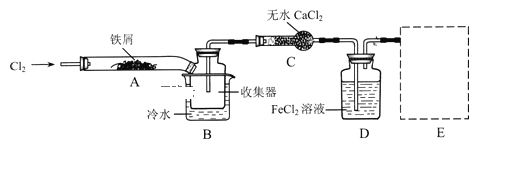
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④…
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封.
请回答下列问题:
(1)装置A中反应的化学方程式为 _______________________
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端.要使沉积的FeCl3进入收集器,第④步操作是 ________________________
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号) _________________________
(4)装置B中冷水浴的作用为;_________装置C的名称为 ______________;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂:__________________________
(5)在虚线框中尾气吸收装置E所用试剂为____________________________
(6)用含有A12O3、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
V.浓缩、结晶、分离,得到产品。
已知:金属离子的起始浓度为0.1mol·L-1
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 |
完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:______________________________________________________
【题目】下表是元素周期表的一部分,回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | ④ | ||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
⑴①元素的名称:_______,⑧元素的符号:_______;
⑵在这些元素中,最活泼的金属元素的离子结构示意图是____,最活泼的非金属元素是____(填元素符号,下同),____是最不活泼的元素;
⑶这些元素的最高价氧化物对应水化物中,______(填化学式,下同)酸性最强,________碱性最强;能形成两性氢氧化物的元素是____(填元素符号);
⑷在⑤到的元素中,_______(填元素符号)原子半径最小;
⑸⑤和⑦两种元素最高价氧化物对应的水化物相互反应的离子方程式:__________。




