题目内容
下图表示的是向Na2CO3溶液中滴入稀盐酸时产生CO2
的过程。
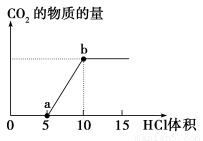
(1)写出a点以前发生反应的离子方程式:_____________________________________
(2)写出a到b点发生反应的离子方程式:_____________________________________
(3)若某Na2CO3溶液中含m mol Na2CO3,向其中滴入一定量的稀盐酸,恰好使溶液中Cl-和HCO的物质的量浓度之比为2∶1,则滴入的稀盐酸中的HCl的物质的量等于________mol(用含字母m的代数式表示)。
(1)CO32—+H+=HCO3—
(2)HCO+H+=CO2↑+H2O (3)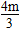
【解析】向Na2CO3溶液中逐滴加入盐酸时,发生的反应依次为
Na2CO3+HCl=NaCl+NaHCO3① NaHCO3+HCl=NaCl+CO2↑+H2O②
(1)a点前发生反应①,离子方程式为:CO32—+H+=HCO3—。
(2)a点到b点发生反应②,离子方程式为:
HCO+H+=CO2↑+H2O。
(3)根据反应①、②,当n(Cl-)∶n(HCO)=2∶1时,Na2CO3部分转化为NaHCO3,所以:
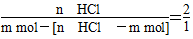 ,
,
解得n(HCl)=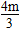 mol。
mol。

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含的离子如下表所示:
阳离子 | NH4+、Na+、Mg2+ |
阴离子 | OH-、NO3—、SO42— |
取等质量的三种化合物配制成相同体积的溶液,其溶质的物质的量浓度:c(甲)>c(乙)>c(丙)。
(1)甲是________,向AlCl3溶液中逐滴加入甲溶液,观察到的现象是________,对应的离子方程式为________。
(2)乙是______,设计实验确定乙的物质组成________(若乙已确定,则不填该空)。