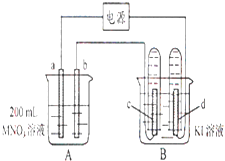
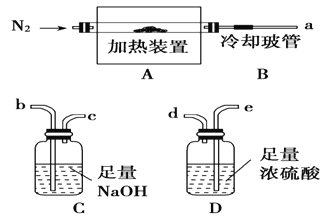
��Ŀ����
����Ŀ�����̰��������װ�(OMS-2)��һ�����͵Ļ��������������̿�ͻ�������Ҫ�ɷֱַ�ΪMnO2��FeS2���ϳ�OMS-2�Ĺ����������£�
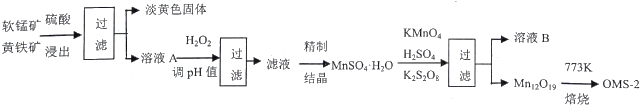
��1��FeS2����Ԫ�صĻ��ϼ���_________������pH�����ˡ���Ҫ��ȥ______Ԫ�ء�
��2��Mn12O19����Ԫ�ػ��ϼ۾�Ϊ-2�ۣ���Ԫ�صĻ��ϼ������֣���Mn (��)��Mn (��) ���ʵ���֮��Ϊ_______________�����������е�ԭ��KMnO4��K2S2O8��MnSO4��H2O�����ʵ�����1:1:5��Ӧ����������Ԫ��ȫ����SO42-����ʽ���ڣ��÷�Ӧ�����ӷ���ʽΪ__________________________��
��3����ҺB�ɽ�һ�������������Ҫ�����һ�ֿ��ڸù�����ѭ��ʹ�ã���ѧʽ��____________����һ��Ϊ���࣬��ũҵ�����п�����___________________________��
��4��OMS-2��һ�������ķ���ɸ���ֱ���OMS-2��MnOx�Լ�ȩ���д�����������ͬʱ���ڼ�ȩת���ʺ��¶ȵĹ�ϵ��ͼ��
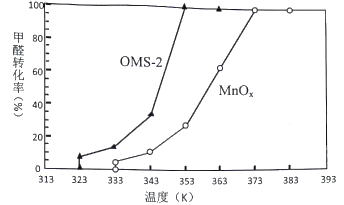
��ͼ��֪��OMS-2��MnOx��ȣ���Ч�ʽϸ���____________________��ԭ����________________��
��5����ȩ(HCHO)��OMS-2����������������CO2��H2O��������OMS-2��ij�ܱտռ�ļ�ȩ���д�����ʵ�飬ʵ�鿪ʼʱ���ÿռ��ڼ�ȩ����Ϊ1.22mg/L��CO2����Ϊ0.590mg/L��һ��ʱ�����CO2����������1.25mg/L����ʵ���м�ȩ��ת����Ϊ_______________________��
���𰸡� -1 Fe���� 5:1 2MnO4-+ 2S2O82-+10Mn2++11H2O=Mn12O19��+4SO42-+22H+ H2SO4 ���� OMS-2 OMS-2 ��MnOx������������ķ�Ӧ��Ũ�ȸ��ߣ���Ӧ���ʸ��� 36.9%
�����������������̰��������װ�(OMS-2)�ĺϳ�Ϊ���忼�鹤������ͼ�����ڿ���ѧ�����ۺϷ�����������1��FeS2����Ԫ�صĻ��ϼ�Ϊ+2�ۣ���Ԫ�صĻ��ϼ���-1�����̿�ͻ�����������������ҺA�к���Fe2+������H2O2��Fe2+����ΪFe3+������pH����Ԫ�س�ȥ�õ�MnSO4��H2O����2��Mn12O19����Ԫ�ػ��ϼ۾�Ϊ-2�ۣ���Mn (��)Ϊx������Mn (��)Ϊ12-x�����ݻ�������Ԫ�ػ��ϼ۴�����Ϊ0������3x+4(12-x)=2��19,xΪ10��Mn (��)Ϊ2��Mn (��)��Mn (��) ���ʵ���֮��Ϊ5:1�������������������е�ԭ��KMnO4��K2S2O8��MnSO4��H2O�����ʵ�����1:1:5��Ӧ����������Ԫ��ȫ����SO42-����ʽ���ڣ��÷�Ӧ�����ӷ���ʽΪ2MnO4-+ 2S2O82-+10Mn2++11H2O=Mn12O19��+4SO42-+22H+����3�����ݷ�Ӧ����ʽ��֪����ҺB�к��е�K2SO4��H2SO4���ù�����ѭ��ʹ�õ����ʻ�ѧʽ��H2SO4��K2SO4��ũҵ�����п������طʣ���4����ͼ����Կ�������ͬ�¶��£�OMS-2������ʱ��������OMS-2 ��MnOx������������ķ�Ӧ��Ũ�ȸ��ߣ���Ӧ���ʸ��죬��OMS-2��MnOx��ȣ���Ч�ʽϸ���OMS-2����5�������ΪVL��CO2������0.590mg/L������1.25mg/L��CO2��������0.66mg/L����Ӧ���ɵ�CO2�����ʵ���Ϊ![]() ������ԭ�Ӹ����غ㣬���뷴Ӧ�ļ�ȩ�����ʵ���Ϊ
������ԭ�Ӹ����غ㣬���뷴Ӧ�ļ�ȩ�����ʵ���Ϊ![]() ���ʸ�ʵ���м�ȩ��ת����Ϊ
���ʸ�ʵ���м�ȩ��ת����Ϊ =36.9%��
=36.9%��

 ����С����ͬ������ϵ�д�
����С����ͬ������ϵ�д�����Ŀ����0.1032molL��1 HCl��Һ�ζ�δ֪Ũ�ȵ�NaOH��Һ��
��1��ijͬѧ�����в������ʵ�飺��ȡһ��ƿ���ô���NaOH��Һ��ϴ���Σ� ������ƿ�м��� 25��.00 mL����NaOH��Һ���ۼ��뼸��ʯ���Լ���ָʾ������ȡһ֧��ʽ�ζ��ܣ�ϴ�Ӹɾ��� ��ֱ������ʽ�ζ�����ע�������Һ�����еζ��� ������ע���ŵζ�����������ҺҺ���½���ֱ���ζ��յ㣮
�������������д�������Ϊ
��2��ȡ��25.00 mL����NaOH��ҺӦ��������ѡ����ס������ҡ���װ�ã���ȡ��NaOH��Һ��ʼƽ�Ӷ���������ʱ���Ӷ������ᵼ����������������ҺŨ�����ƫ��ƫС�����䡰�� ![]()
��3�����ζ���ʼǰ�ζ��ܼ�������һ���ݣ��ζ�������������ʧ�� ��ᵼ����������������ҺŨ�����ƫ��ƫС�����䡰��
��4����ƽ��ʵ�����Σ���¼���������±�
�ζ����� | ������Һ�������/mL�� | ��HCl��Һ����� | |
�ζ�ǰ������/mL�� | �ζ��������/mL�� | ||
�� | 25.00 | 1.02 | 21.04 |
�� | 25.00 | 2.00 | 22.98 |
�� | 25.00 | 0.20 | 20.18 |
�Լ������NaOH��Һ�����ʵ���Ũ�ȣ��г�������̣���