题目内容
【题目】【题目】氯离子插层镁铝水滑石[Mg2Al(OH)6Cl·xH2O]是一种新型离子交换材料,其在高温下完全分解为MgO、Al2O3、HCl和水蒸气。现用下图装置进行实验确定其化学式(固定装置略去)。
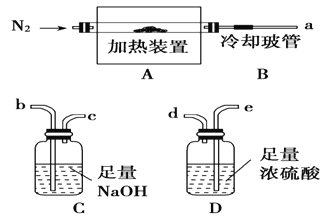
(1)Mg2Al(OH)6Cl·xH2O热分解的化学方程式___________________________。
(2)若只通过测定装置C、D的增重来确定x,则装置的连接顺序为________(按气流方向,用接口字母表示),其中C的作用是________。装置连接后,首先要进行的操作的名称是________。
(3)加热前先通N2排尽装置中的空气,称取C、D的初始质量后,再持续通入N2的作用是______________________、_________________等。
(4)完全分解后测得C增重3.65 g、D增重9.90 g,则x=________。若取消冷却玻管B后进行实验,测定的x值将________(填“偏高”或“偏低”)。
(5)上述水滑石在空气中放置时易发生反应生成[Mg2Al(OH)6Cl1-2y·(CO3)y·zH2O],该生成物能发生类似的热分解反应。现以此物质为样品,用(2)中连接的装置和试剂进行实验测定z,除测定D的增重外,至少还需测定___________。
【答案】 2[Mg2Al(OH)6Cl·xH2O==4MgO+Al2O3+2HCl↑+(5+2x)H2O↑ aedb 吸收HCl气体 检查气密性 将分解产生的气体全部带入装置C、D中完全吸收 防止产生倒吸 3 偏低 装置C的增重及样品质量(样品质量及样品分解后残余物质量或装置C的增重及样品分解后残余物质量)
【解析】(1)从题目可以知道,[Mg2Al(OH)6Cl·xH2O]在高温下完全分解为MgO+Al2O3+HCl和水蒸气,分解产物已经确定,配平即可得到化学方程式。
(2)x是结晶水的系数,确定x需要测定分解产物中水蒸气的质量及![]() 气体的质量,则需先用浓硫酸来吸收尾气中的水蒸气,然后NaOH吸收HCl,通过浓硫酸的增重来计算水蒸气,再通过NaOH溶液的增重来计算HCl,且顺序不能颠倒,因为尾气先经NaOH溶液会带出部分水蒸气,造成较大误差,故连接顺序为aedb;NaOH与酸性气体HCl发生反应,故C的作用是吸收HCl气体;这个反应有大量气体生成,实验前必须检查实验装置的气密性,故首先要进行的操作的名称是检查气密性。
气体的质量,则需先用浓硫酸来吸收尾气中的水蒸气,然后NaOH吸收HCl,通过浓硫酸的增重来计算水蒸气,再通过NaOH溶液的增重来计算HCl,且顺序不能颠倒,因为尾气先经NaOH溶液会带出部分水蒸气,造成较大误差,故连接顺序为aedb;NaOH与酸性气体HCl发生反应,故C的作用是吸收HCl气体;这个反应有大量气体生成,实验前必须检查实验装置的气密性,故首先要进行的操作的名称是检查气密性。
(3)N2不会与体系的任一物质发生反应,故持续通入N2能把分解的气体全部带入装置C、D,另外,反应中产生的气体都被吸收,容易造成倒吸,持续通入![]() 能防止产生倒吸。
能防止产生倒吸。
(4)由化学方程式可知水蒸气和HCl气体的比例关系为: ![]() ,故x=3;若取消冷却玻管B后进行实验,温度过高的水蒸气会影响装置D浓硫酸的吸收,由比例关系式:
,故x=3;若取消冷却玻管B后进行实验,温度过高的水蒸气会影响装置D浓硫酸的吸收,由比例关系式: ![]() 可知,x的值会偏低。
可知,x的值会偏低。
(5)[Mg2Al(OH)6Cl1-2y·(CO3)y·zH2O]与[Mg2Al(OH)6Cl·xH2O]的高温分解反应类似,但还有无法用上述装置测量的H2,故除了装置D的增重,还需测量另外两个变化量,如测量样品质量、样品分解后残余物质量和装置C的增重,故还需测量装置C的增重及样品质量(样品质量及样品分解后残余物质量或装置C的增重及样品分解后残余物质量)。

 名校课堂系列答案
名校课堂系列答案