��Ŀ����
����Ŀ��������һ����Ҫ�Ļ���ԭ�ϣ���������������Ӧ��ʮ�ֹ㷺���ؿ�����ȡ�����ķ�ӦΪ��4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)��H= -120kJ/mol �÷�Ӧ���������У������ԭ������ͼ��ʾ��
2Cl2(g)+2H2O(g)��H= -120kJ/mol �÷�Ӧ���������У������ԭ������ͼ��ʾ��

���� I �ķ�ӦΪ�� 2HCl(g)+CuO(s) ![]() CuCl2(s)+H2O(g)��H= -132kJ/mol
CuCl2(s)+H2O(g)��H= -132kJ/mol
(1)��ԭ���������������ʵĻ�ѧʽΪ_______________________��
(2)���� II ��Ӧ���Ȼ�ѧ����ʽΪ____________________��
(3)ѹǿΪp1ʱ���ؿ�����HCl ��ƽ��ת����aHCl ���¶ȱ仯������ͼ��

�ٱȽ� a��b �����ƽ�ⳣ����С K(a)=_______________K(b)(����>����<������=��)������ԭ��Ϊ________________��
��c ���ʾͶ�ϲ��䣬 350�桢ѹǿΪp2ʱ���ؿ�����HCl ��ƽ��ת���ʣ���p2_________________p1(����>����<������=��)��
���𰸡�CuO 2CuCl2(s)+ O2(g) = 2CuO(s) + 2C12(g)��H= +144kJ/mol �� �����¶�HCl��ת���ʽ���,��ƽ�������ƶ���ƽ�ⳣ����С ��
��������
(1).���ݷ�Ӧǰ��CuO���仯��֪CuOΪ������
(2).���ݸ�˹���ɽ��
(3).����Ӱ��ƽ���ƶ���������¶�HCl��ת���ʽ��ͣ���ƽ�������ƶ���ƽ�ⳣ����С��
(1)����ͼ֪����ӦI��CuO�Ƿ�Ӧ���ӦII��CuO�����������CuOΪ�������ʴ�Ϊ: CuO��
(2) ��4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)��H= -120kJ/mol
2Cl2(g)+2H2O(g)��H= -120kJ/mol
��2HCl(g)+CuO(s) ![]() CuCl2(s)+H2O(g)��H= -132kJ/mol
CuCl2(s)+H2O(g)��H= -132kJ/mol
��ӦII�ķ���ʽΪ2CuCl2(s)+ O2(g) = 2CuO(s) + 2C12(g)������ʽII���ɢ�- 2���ڵõ�����H= - 120kJ/mol- 2��(-132kJ/mol)= + 144kJ/ mol���ʴ�Ϊ��2CuCl(s)+ O2(g) = 2CuO(s) + 2C12(g)��H= +144kJ/mol��
(3)�������¶�HCl��ת���ʽ��ͣ���ƽ�������ƶ���ƽ�ⳣ����С��ѹǿ��ͬʱ�¶�a< b����K(a)> K(b)���ʴ�Ϊ: > �������¶�HCl��ת���ʽ��ͣ���ƽ�������ƶ���ƽ�ⳣ����С��
��c���ʾͶ�ϲ��䣬350�桢ѹǿΪp2ʱ���÷�Ӧǰ�����������֮�ͼ�С������ѹǿHCl��ת����������ͬ�¶�ʱת����c��ͣ���c��ѹǿ��С������p2<p1���ʴ�Ϊ: <��

����Ŀ������ʵ����,���ó��Ľ�����ȷ����()
ʵ�� | ���� | ���� | |
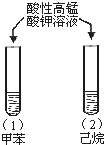
A |
| �Թ�(1)����ɫ��ȥ, �Թ�(2)����ɫδ�� | ��ʹ�����Ļ�����ǿ |
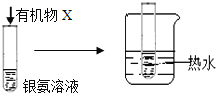
B |
| �Թ��ڱ��� �������� | �л���X��һ������ȩ�� |
C | �������Һ�м���ϡ����,ˮԡ����,һ��ʱ���,�ټ������Ƶ�������ͭ����Һ������ | δ��ש��ɫ���� | ����δˮ�� |
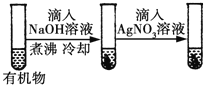
D |
| ���һֻ�Թ�����dz��ɫ���� | �л����к�����ԭ�� |
A.AB.BC.CD.D