题目内容
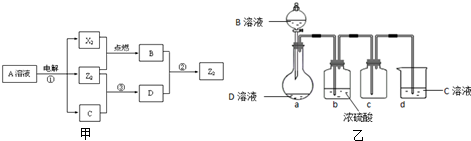
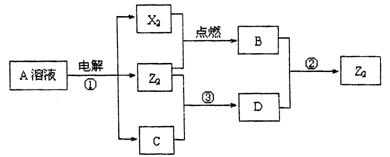
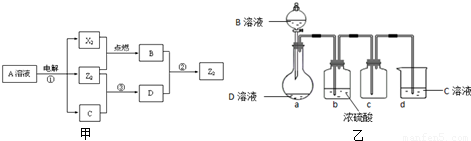
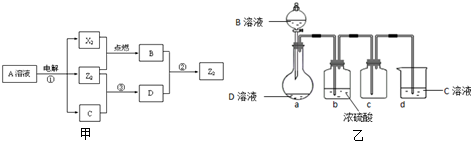
已知下列物质之间能实现如图甲所示的转化关系(部分产物已略去):
(1)Z2的结构式是______.反应①的离子方程式是______;
(2)反应③的离子方程式是______.
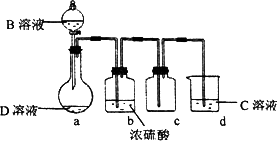
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应.某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如图乙所示(夹持固定装置的仪器已略去).
I、写出反应②的离子方程式______.
II、上述实验装置不够完善,改进方法是______.
Ⅲ、足量Z2 通入FeBr2溶液中发生反应的离子方程式是______.
解:由反应①A溶液在电解的情况下生成3中物质,其中两种物质为双原子分子,A可能为氯化物(阳离子不放电),C为碱溶液;B为HCl,z2+碱→D,故z2为Cl2,结合反应②可知D为次氯酸盐,符合转化关系,
(1)由上述分析可知,z2为Cl2,结构式为Cl-Cl;反应①电解氯化物溶液生成碱、氯气、氢气,反应离子方程式为:
2 Cl-+2H2O 2OH-+Cl2↑+H2↑;
2OH-+Cl2↑+H2↑;
故答案为:Cl-Cl;2 Cl-+2H2O 2OH-+Cl2↑+H2↑;
2OH-+Cl2↑+H2↑;
(2)氯气与碱反应生成氯化物、次氯酸盐、水,反应③的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(3)Ⅰ、在酸性条件下,Cl-与ClO-生成Cl2与水,反应离子方程式为:ClO-+Cl-+2H+=Cl2↑+H2O;
故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
Ⅱ、反应②为Cl-+ClO-→Cl2,利用装置乙制备纯净、干燥的Cl2,HCl易挥发,故制备的氯气中含有HCl、水蒸气,先利用饱和的氯化钠溶液吸收HCl,再利用浓硫酸干燥,可得纯净、干燥的Cl2,氯气有毒,污染大气,故最后利用氢氧化钠溶液吸收尾气中的氯气,由装置图可知,缺少吸收HCl的装置,故在a、b装置之间加一盛有饱和食盐水的洗气瓶,除去HCl;
故答案为:在a、b装置之间加一盛有饱和食盐水的洗气瓶,除去HCl;
Ⅲ、氯气具有强氧化性,将亚铁离子氧化为铁离子,将溴离子氧化为Br2,足量的氯气,溶液中Fe2+、Br-全部被氧化,反应离子方程式为:2 Fe2++4Br-+3Cl2=6Cl-+2 Fe3++2Br2;
故答案为:2 Fe2++4Br-+3Cl2=6Cl-+2 Fe3++2Br2.
分析:(1)(2)由反应①A溶液在电解的情况下生成3中物质,其中两种物质为双原子分子,A可能为氯化物(阳离子不放电),C为碱溶液;B为HCl,z2+碱→D,故z2为Cl2,结合反应②可知D为次氯酸盐,验证符合转化关系;
(3)Ⅰ、在酸性条件下,Cl-与ClO-生成Cl2与水;
Ⅱ、反应②为Cl-+ClO-→Cl2,利用装置乙制备纯净、干燥的Cl2,HCl易挥发,故制备的氯气中含有HCl、水蒸气,先利用饱和的氯化钠溶液吸收HCl,再利用浓硫酸干燥,可得纯净、干燥的Cl2,氯气有毒,污染大气,故最后利用氢氧化钠溶液吸收尾气中的氯气;
Ⅲ、氯气具有强氧化性,将亚铁离子氧化为铁离子,将溴离子氧化为Br2,足量的氯气,溶液中Fe2+、Br-全部被氧化.
点评:以“无机框图题”的形式考查元素单质及其化合物的性质、氯气的制备实验,涉及常用化学用语、氧化还原反应等,难度中等,根据电解产物的特点,推断A是突破口与解题的关键.
(1)由上述分析可知,z2为Cl2,结构式为Cl-Cl;反应①电解氯化物溶液生成碱、氯气、氢气,反应离子方程式为:
2 Cl-+2H2O
 2OH-+Cl2↑+H2↑;
2OH-+Cl2↑+H2↑;故答案为:Cl-Cl;2 Cl-+2H2O
 2OH-+Cl2↑+H2↑;
2OH-+Cl2↑+H2↑;(2)氯气与碱反应生成氯化物、次氯酸盐、水,反应③的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(3)Ⅰ、在酸性条件下,Cl-与ClO-生成Cl2与水,反应离子方程式为:ClO-+Cl-+2H+=Cl2↑+H2O;
故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
Ⅱ、反应②为Cl-+ClO-→Cl2,利用装置乙制备纯净、干燥的Cl2,HCl易挥发,故制备的氯气中含有HCl、水蒸气,先利用饱和的氯化钠溶液吸收HCl,再利用浓硫酸干燥,可得纯净、干燥的Cl2,氯气有毒,污染大气,故最后利用氢氧化钠溶液吸收尾气中的氯气,由装置图可知,缺少吸收HCl的装置,故在a、b装置之间加一盛有饱和食盐水的洗气瓶,除去HCl;
故答案为:在a、b装置之间加一盛有饱和食盐水的洗气瓶,除去HCl;
Ⅲ、氯气具有强氧化性,将亚铁离子氧化为铁离子,将溴离子氧化为Br2,足量的氯气,溶液中Fe2+、Br-全部被氧化,反应离子方程式为:2 Fe2++4Br-+3Cl2=6Cl-+2 Fe3++2Br2;
故答案为:2 Fe2++4Br-+3Cl2=6Cl-+2 Fe3++2Br2.
分析:(1)(2)由反应①A溶液在电解的情况下生成3中物质,其中两种物质为双原子分子,A可能为氯化物(阳离子不放电),C为碱溶液;B为HCl,z2+碱→D,故z2为Cl2,结合反应②可知D为次氯酸盐,验证符合转化关系;
(3)Ⅰ、在酸性条件下,Cl-与ClO-生成Cl2与水;
Ⅱ、反应②为Cl-+ClO-→Cl2,利用装置乙制备纯净、干燥的Cl2,HCl易挥发,故制备的氯气中含有HCl、水蒸气,先利用饱和的氯化钠溶液吸收HCl,再利用浓硫酸干燥,可得纯净、干燥的Cl2,氯气有毒,污染大气,故最后利用氢氧化钠溶液吸收尾气中的氯气;
Ⅲ、氯气具有强氧化性,将亚铁离子氧化为铁离子,将溴离子氧化为Br2,足量的氯气,溶液中Fe2+、Br-全部被氧化.
点评:以“无机框图题”的形式考查元素单质及其化合物的性质、氯气的制备实验,涉及常用化学用语、氧化还原反应等,难度中等,根据电解产物的特点,推断A是突破口与解题的关键.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目