题目内容


(2)已知某粒子的结构示意图为:

试回答:
①当x-y=10时,该粒子为
②当y=8时,粒子可能为(填名称)
③写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式
(2)①核电荷数等于核外电子数的微粒为原子;
②18电子的单核微粒包括原子、阴离子和阳离子几种情况;
③氢氧化铝具有两性,可以和强酸反应.
| 3y |
| 5 |
 ,故答案为:
,故答案为: ;
;(2)①当x-y=10时,x=10+y,说明核电荷数等于核外电子数,所以该粒子应为原子,故答案为:原子;
②当y=8时,应为有18个电子的单核粒子,所以可能为氩原子、氯离子、硫离子、钾离子、钙离子,故答案为:氩原子、氯离子、硫离子、钾离子、钙离子;
③y=3时为铝原子、y=7时为氯原子,其最高价氧化物对应的水化物分别为氢氧化铝和高氯酸,氢氧化铝和强酸反应的实质是:Al(OH)3+3H+═Al3++3H2O,故答案为:Al(OH)3+3H+═Al3++3H2O.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(7分)元素周期表是学习物质结构和性质的重要工具,下面是元素周期表的一部分,表中所列字母A、D、E、G、Q、M、R、T分别代表某一化学元素。请用所给元素回答下列问题。
| A | | | |||||||||||||||
| | | | | D | E | | | | |||||||||
| G | | | Q | | M | R | | ||||||||||
| | | | | | | | T | | | | | | | | | | |
 (2)某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号) 。
(2)某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号) 。(3)M、D两种元素形成的化合物含有的化学键类型是 ,其分子是(填“极性”或“非极性”) 分子;
A分别与D、E、R形成的分子中,分子间存在氢键的是(填分子式) 。
A与D形成分子的空间结构可能是(填序号) 。(2分)

(7分)元素周期表是学习物质结构和性质的重要工具,下面是元素周期表的一部分,表中所列字母A、D、E、G、Q、M、R、T分别代表某一化学元素。请用所给元素回答下列问题。
|
A |
|
|
|||||||||||||||
|
|
|
|
|
D |
E |
|
|
|
|||||||||
|
G |
|
|
Q |
|
M |
R |
|
||||||||||
|
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
(1)某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为 。
 (2)某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)
。
(2)某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)
。
(3)M、D两种元素形成的化合物含有的化学键类型是 ,其分子是(填“极性”或“非极性”) 分子;
A分别与D、E、R形成的分子中,分子间存在氢键的是(填分子式) 。
A与D形成分子的空间结构可能是(填序号) 。(2分)

元素周期表是学习物质结构和性质的重要工具,下面是元素周期表的一部分,表中所列字母A、D、E、G、Q、M、R、T分别代表某一化学元素。请用所给元素回答下列问题。
| A | |||||||||||||||||
| D | E | ||||||||||||||||
| G | Q | M | R | ||||||||||||||
| T | |||||||||||||||||
(1)某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为 。
![]() (2)某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号) 。
(2)某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号) 。
(3)M、D两种元素形成的化合物含有的化学键类型是 ,其分子是(填“极性”或“非极性”) 分子;A分别与D、E、R形成的分子中,分子间存在氢键的是(填分子式) 。A与D形成分子的空间结构可能是(填序号) 。
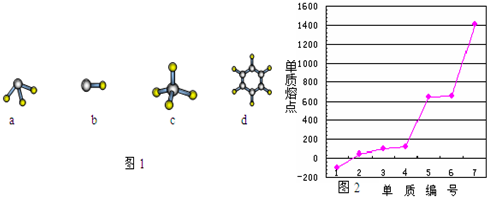
a b c d
图1
(4)从所给元素中组成合适的反应物,用化学方程式表明元素M、R的非金属性强弱:
。
(5)第三周期主族元素单质熔点高低的顺序如图2所示,“1”所代表物质的化学式是 ,“7”所对应的元素形成最高价氧化物的晶体类型是 。

图2